等物质的量的下列金属分别跟足量盐酸反应,同温同压下产生氢气体积最大的是
| A.钠 | B.铝 | C.镁 | D.铁 |
NA表示阿伏加德罗常数的值。下列判断正确的是
| A.常温常压下,17g氨气分子所含质子数为10NA |
| B.1mol Cl2参加反应,转移电子数一定为2NA. |
| C.常温常压下,22.4 L CO2分子中含有2NA个σ键和2NA个1π键 |
| D.1 L 0. 01 mol.L-1的Na2CO3溶液中含有0.01NA个CO32- |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.用石墨作电极电解饱和食盐水时,若阴极得到2NA个电子,则阳极产生22.4 L气体 |
| B.2 L 0.05 mol/L乙酸溶液中H+数为0.1NA |
| C.等物质的量的Na2O和Na2O2中含有的阴离子总数不同 |
| D.常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.4NA |
某溶液中含有NH4+、Mg2+、Fe2+、A13+和SO42—五种离子,若向其中加入过量的Ba(OH)2溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有
| A.4种 | B.3种 | C.2种 | D.1种 |
若司机酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应如下:2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O。关于该反应,下列叙述不正确的是
| A.每1molCrO3发生氧化反应,转移3mole— |
| B.C2H5OH是还原剂 |
| C.CrO3在反应中表现氧化性 |
| D.C2H5OH在反应中失去电子 |
下列化学用语正确的是
A.CH4分子的球棍模型: |
| B.乙烯的结构简式:CH2CH2 |
| C.氯化钠的分子式:NaCl |
D.K+的结构示意图: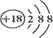 |