美日科学家因在研究“钯催化交叉偶联反应”所作出的杰出贡献,获得了2010年诺贝尔化学奖。钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,该反应的反应物与生成物有:CO、Pd、H2O、HCl、PdCl2和一种未知物X。下列说法不正确的是
| A.反应中CO作还原剂 |
| B.未知物质X为CO2 |
| C.反应中转移的电子为1mol时,生成2mol物质X |
| D.题述反应条件下还原性:CO>Pd |
下列反应或过程属于吸热的是
| A.盐酸与NaOH溶液的反应 | B.H + H= H2 |
| C.Al和Fe2O3的铝热反应 | D.Ba(OH)2.8H2O与NH4Cl反应 |
以下说法正确的是
| A.金刚石和石墨可互称为同位素 |
| B.D2和T2可互称为同素异形体 |
C.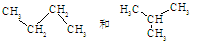 互为同分异构体 互为同分异构体 |
| D.H和D是同素异形体 |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A.质量数为37的氯原子: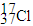 |
B.CH4分子的比例模型: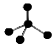 |
| C.H2O的结构式: H—O—H | D.氯化铵的电子式: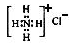 |
二茂铁[(C5H5)2Fe] 分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法正确的是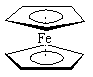
A.二茂 铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键 |
B.1mol环戊二烯(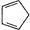 )中含 )中含 有σ键的数目为5NA 有σ键的数目为5NA |
C.分子中存 在π键 在π键 |
D.Fe2+的电子排布式为1s22s22p63s 23p63d44s2 23p63d44s2 |
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是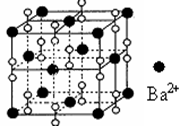
| A.该晶体属于离子晶体 |
| B.晶体的化学式为Ba2O2 |
| C.该晶体晶胞结构与NaCl相似 |
| D.与每个Ba2+距离相等且最近的Ba2+共有12个 |