取相同体积的KI、Na2S和FeBr2溶液分别通入足量的Cl2,当反应恰好完成时,消耗Cl2的体积相同(同温同压下),则KI、Na2S、FeBr2溶液的物质的量浓度之比为
| A.1︰1︰2 | B.2︰1︰3 | C.6︰3︰2 | D.3︰2︰1 |
对于相同体积的K2CO3溶液(浓度为c1) 和 (NH4)2CO3溶液(浓度为c2),若其中CO的物质的量浓度相同,则c1和c2的关系是
| A.c1=c2 | B.c1<c2 | C.c1≥c2 | D.c1>c2 |
一定条件下,在固定容积的密闭容器中,能表示反应X(g)+2Y(g)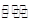 2Z(g)一定达到化学平衡状态的是
2Z(g)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1∶2∶2②X、Y、Z的浓度不再发生变化
③容器中气体的压强不再发生变化④单位时间内生成n mol Z,同时生成n mol X
| A.①② | B.①④ | C.②③ | D.③④ |
《化学反应原理》模块从不同的视角对化学反应进行了探究、分析。以下观点中不正确的是
①放热反应在常温下均能自发进行;②电解过程中,化学能转化为电能而“储存”起来;
③原电池工作时所发生的反应一定有氧化还原反应;④加热时,化学反应只向吸热反应方向进行;
⑤盐类均能发生水解反应;⑥化学平衡常数的表达式与化学反应方程式的书写无关。
| A.①②④⑤⑥ | B.①④⑤⑥ | C.②③⑤⑥ | D.①②④⑤ |
已知温度T时水的离子积常数为KW,该温度下,将浓度为amol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的PH=7 |
C.混合溶液中,c(H+)=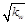 mol·L-1 mol·L-1 |
| D.混合溶液中,c(H+)+ c(B+)= c(OH-)+ c(A-) |
下列实验操作正确的是
| A.用pH试纸测得某新制氯水的pH值为3.5 |
| B.电解法精炼铜,将粗铜接电源的正极 |
| C.将氯化铁晶体溶于蒸馏水中,配制氯化铁溶液 |
| D.将氯化铁溶液加热蒸干,再灼烧,就得到氯化铁晶体 |