下列各组物质中,物质之间通过一步反应就能实现如图所示的变化的是( ) 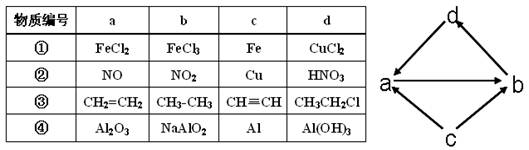
| A.①②③ | B.①③④ | C.①②③④ | D.②④ |
下列说法不正确的是
| A.将一块未擦去氧化膜的铝片放入适量0.5mol·L-1CuSO4溶液中,铝片表面无明显现象 |
| B.向其中一支试管中加入1mL乙醇,向另一支试管中加入约1.5g苯酚。再向上述两支试管中各加一小块吸干煤油的金属钠,比较乙醇和苯酚中羟基上氢原子的活泼性 |
| C.用新制氢氧化铜可以检验牙膏中是否含有甘油,新制氢氧化铜与甘油反应生成绛蓝色溶液 |
| D.用稀KMnO4酸性溶液可以检验火柴头燃烧时是否产生了二氧化硫气体 |
下列说法不正确的是
| A.可用FeCl3溶液检验阿司匹林中是否含有未反应完的水杨酸 |
| B.当沉淀的结晶颗粒较大,静置后容易沉降至容器底部时,常用倾析法分离或洗涤 |
| C.在硫酸亚铁铵制备实验中,用少量酒精洗去晶体表面附着的水分;在阿司匹林的制备实验中用冷水洗涤阿司匹林 |
| D.把等物质的量浓度的硫酸铵和硫酸亚铁混合,搅拌,小火加热,在蒸发皿中蒸发至有大量晶体析出,即可得硫酸亚铁铵晶体 |
下列说法不正确的是
| A.纸层析法实验中,应使点有试样的滤纸末端浸入展开剂中约0.5cm,注意不要让试样点接触展开剂 |
| B.将一定浓度的硝酸钠和氯化钾溶液混合加热至沸腾,使溶液浓缩,有晶体析出,趁热过滤,得到的晶体是氯化钠,将滤液冷却,可使硝酸钾晶体析出 |
| C.晶体颗粒的大小与结晶条件有关,溶质的溶解度越大,或溶液的浓度越高,或溶剂的蒸发速度越快,或溶液冷却得越快,析出的晶粒就越细小 |
| D.当溶液发生过饱和现象时,振荡容器,用玻璃棒搅动或轻轻地摩擦器壁,或投入几粒晶体,都可促使晶体析出 |
下列说法不正确的是
| A.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
| B.在中和滴定实验中,既可用标准溶液滴定待测液,也可用待测液滴定标准溶液 |
| C.实验中需用2.0 mol·L-1的Na2 CO3溶液950 mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为950mL,201.4 g |
| D.减压过滤的原理是抽气泵给吸滤瓶减压,造成吸滤瓶内与布氏漏斗液面上的压力差,从而加快过滤速度 |
下列说法不正确的是
| A.利用分液漏斗进行分液操作时,先打开分液漏斗旋塞,使下层液体慢慢流出,待下层液体完全流出后,关闭旋塞,上层液体再从上面倒出 |
| B.用玻璃棒蘸取新制氯水,滴在pH 试纸上,然后与比色卡对照,可测定新制氯水的pH 值 |
| C.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和碱正好反应、取2—3 次的实验平均值,以达到良好的实验效果 |
| D.固体药品取用:块状固体用镊子夹取,粉末状的用药匙或纸槽转移 |