往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生。下列说法不正确的是( )
| A.该实验表明SO2有漂白性 | B.白色沉淀为BaSO4 |
| C.该实验表明FeCl3有氧化性 | D.反应后溶液酸性增强 |
下列烧杯中盛放的都是稀硫酸,在铜电极上能产生气泡的是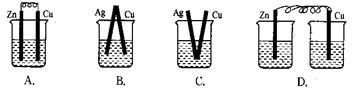
以下分离或提纯的方法中正确的是()
| A.分离碘水中的碘——升华 | B.分离白酒中的酒精和水——分液 |
| C.除去海盐中的硫酸盐——溶解后加硝酸钡 | D.分离海水中的水——蒸馏 |
下列溶液中的Cl-浓度与50 mL 1 mol ·L-1 MgCl2溶液中的Cl-浓度相等的是()
| A.150 mL 1 mol·L-1 NaCl溶液 | B.75 mL 0.5mol·L-1CaCl2溶液 |
| C.150 mL 2 mol·L-1 KCl溶液 | D.75 mL 1 mol ·L-1AlCl3溶液 |
下列各项中表达正确的是()
A.F原子结构示意图: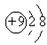 |
B.H2O的电子式: |
| C.1H、2H、3H是三种不同元素 | D.乙烯的分子式: C2H4 |
区别溶液和胶体最简单的方法是()
| A.观察外观 | B.丁达尔效应 | C.布朗运动 | D.加热 |