下列各组物质中,化学键类型完全相同的是( )
| A.N2H4和H2O2 | B.Mg3N2和NaOH |
| C.CCl4和H2O2 | D.Na2O2和NaOH |
镍镉可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:
Cd+2NiOOH+2H2O 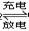 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
由此可知,该电池放电时的负极是 ()
| A.Cd | B.NiOOH | C.Cd(OH)2 | D.Ni(OH)2 |
下列各组离子在给定条件下能大量共存的是 ()
| A.在pH=1的溶液中:NH4+、K+、ClO-、Cl- |
| B.有SO42-存在溶液中:Na+、Mg2+、Ba2+、I- |
| C.在酸性溶液中:NH4+、Ba2+、Fe2+、NO3- |
| D.在c(H+)=1.0×10-13mol/L的溶液中:Na+、S2-、AlO2-、SO32- |
下列溶液一定是碱性的是 ()
| A.pH = 8的某电解质溶液 | B.c(OH-)>1×10-7mol/L |
| C.溶液中含有OH-. | D.溶液中c(OH-)>c(H+) |
在反应2A+B=3C+4D中,表示该反应速率最快的是 ()
A. v(A)=0.5mol/(L·s)B. v(B)="0.3" mol/(L·s)
C. v(C)="0.8" mol/(L·s) D. v(D)="1" mol/(L·s)
下列各式中属于正确的水解反应的离子方程式的是 ( )
A.CH3COOH + OH-  CH3COO-+H2O CH3COO-+H2O |
B.S2-+2H2O H2S+2OH- H2S+2OH- |
C.CH3COOH+H2O CH3COO-+H3O+ CH3COO-+H3O+ |
D.NH4++H2O NH3· H2O+H+ NH3· H2O+H+ |