.短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是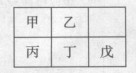
| A.原子半径: 丙<丁<戊 | B.金属性:甲>丙 |
| C.氢氧化物碱性:丙>丁>戊 | D.最外层电子数:甲>乙 |
标准状况下,32gCH4所占体积约为
| A.44.8L | B.22.4L | C.11.2L | D.5.6L |
鉴别稀硫酸和浓硫酸既简单又安全的方法是
| A.各取少量于试管中加入几片铜片 |
| B.用玻璃棒各蘸少许点在滤纸上 |
| C.各取少量于试管中滴加NaOH溶液 |
| D.各取少量于试管中滴加BaCl2溶液 |
日常生活和工业生产中常用到漂白剂。下列物质没有漂白作用的是
| A.HClO | B.SO2 | C.新制氯水 | D.CaCl2 |
2molFeCl2与1molCl2恰好完全反应,则产物的物质的量为
| A.1mol | B.2mol | C.3mol | D.4mol |
下列物质的排放不污染空气的是
| A.燃煤烟气 | B.餐厨油烟 | C.汽车尾气 | D.锅炉水蒸汽 |