张南同学想测定赤铁矿中氧化铁的质量分数,做法如下,请回答下列问题。
(1)配制稀硫酸。
①配制200g 19.6%的稀硫酸,需要98%的浓硫酸的体积是 ;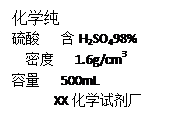
②下图实验过程中出现操作的错误是 。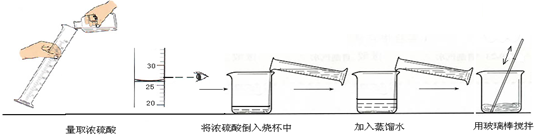
(2)将赤铁矿粉末,用稀硫酸溶解,反应的化学方程式是 ;
(3)取20g的赤铁矿粉末恰好与l50g的19.6%的稀硫酸完全反应,求解生成硫酸铁质量(x)的比例式为 ;
(4)此赤铁矿中氧化铁的质量分数为 ;
(5)向反应后所得溶液中加入34g水,则所得溶液溶质的质量分数是
有铁粉和铜粉的均匀混合物,甲、乙、丙三位同学分别取该混合物与稀硫酸反应,所得数据如下表所示:
| 甲 |
乙 |
丙 |
|
| 取用金属混合物的质量/ | 10 |
10 |
20 |
| 取用稀硫酸的质量/ | 100 |
120 |
100 |
| 反应后过滤,得干燥固体的质量/ | 4 |
4 |
13 |
请分析数据,回答下列问题:
(1)甲所得溶液中含有溶质的是。
(2)根据实验数据分析,若取用金属混合物15
,加入到120
稀硫酸中,充分反应后最终得到固体质量为
。
(3)计算丙同学所得溶液中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)
锌是人体健康所必需的元素,葡萄糖酸锌是一种常用的补锌剂。下图是某品牌葡萄糖酸锌口服液的标签。
请根据标签信息回答问题:
(1)葡萄糖酸锌(相对分子质量为455)中锌元素的质量分数为(精确到0.1%)
(2)某患者除正常饮食吸收锌元素外,还需要服用该品牌葡萄糖酸锌口服液。若治疗一个疗程需要补充113mg锌元素,而这些锌有75%来自该口服液,则患者共需要服用支葡萄糖酸锌口服液。
| XX牌口服液 主要成分:葡萄糖酸锌 化学式: 含量:每支口服液含葡萄糖酸锌24.7mg 用法及用量:口服,…6岁以上每日2次,每次1支… XX制药厂 |
氢氧化钙长期存放容易变质。某科学探究小组在实验时取了一瓶存放多年的氢氧化钙来检验其变质情况。首先取氢氧化钙样品12.2g于锥形瓶中,加入32.8g水,充分振荡形成悬浊液,然后向锥形瓶中逐滴滴加29. 2%的盐酸使其充分反应。实验测得加入盐酸的质量与锥形瓶中物质的质量关系如下图所示。
求:(1)图中AB段与盐酸反应的物质是____
(2)图中BC段发生反应的化学方程式为
(3)样品中氢氧化钙的质量分数(精确到0.1,写出计算过程)。
人体缺少钙元素会影响健康,因此每日需摄人足够的钙。市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算。
(1)葡萄糖酸钙相对分子质量为
(2)葡萄糖酸钙中氢、氧元素的质量比为
(3)按说明书服用钙片时,每天能够补充的钙为mg(精确到0.1)。
右图是实验室中一瓶过氧化氢溶液的标签。某同学为了测定该溶液中溶质的质量分数是否与标签上相符,用烧杯取该溶液50
,加入二氧化锰1
,完全反应后,称得烧杯内剩余物总质量为49.4
。请回答下列问题:
(1)二氧化锰在反应中的作用是。
(2)完全反应后生成氧气的质量为。
(3)通过计算回答,该氧化氢溶液中溶质的质量分数是否与标签上相符?