向质量为30g的Fe、Fe2O3混合物中加人250mL 4mol/L的稀HNO3恰使混合物完全溶解,放出NO(标准状况)2.24L,所得溶液中再滴加KSCN溶液,无血红色出现。若用与上述混合物中铁元素质量相等的铁屑和足量的稀硫酸充分反应,所得到的气体在标准状况下的体积为( )
| A.15.12L | B.l0.08L | C.2.24L | D.3.36L |
COCl2 (g) CO(g)+ Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+ Cl2(g) △H>0,当反应达到平衡时,下列措施①升温②恒容通入惰性气体③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
| A.①②④ | B.①④⑥ | C.②③⑥ | D.③⑤⑥ |
用蒸馏水湿润过的pH试纸测得某氨基酸溶液的pH等于8,则该氨基酸溶液的pH可能是
| A.9 | B.8 | C.7 | D.6 |
关于强弱电解质及非电解质的组合完全正确的是
| A |
B |
C |
D |
|
| 强电解质 |
NaCl |
H2SO4 |
CaCO3 |
HNO3 |
| 弱电解质 |
HF |
氨水 |
HClO |
HI |
| 非电解质 |
Cl2 |
蔗糖 |
C2H5OH |
SO2 |
某反应过程中体系的能量变化如图所示,下列说法错误的是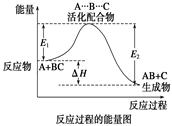
A.反应过程可表示为 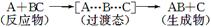 |
| B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能 |
| C.正反应的热效应为ΔH=E1-E2<0,所以正反应为放热反应 |
| D.此图中逆反应的热效应ΔH=E1-E2<0,所以逆反应为放热反应 |
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是
①C(s)+O2(g)=CO2(g)ΔH1C(s)+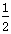 O2(g)=CO(g)ΔH2
O2(g)=CO(g)ΔH2
②S(s)+O2(g)=SO2(g)ΔH3S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+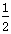 O2(g)=H2O(l)ΔH52H2(g)+O2(g)=2H2O(l)ΔH6
O2(g)=H2O(l)ΔH52H2(g)+O2(g)=2H2O(l)ΔH6
④CaCO3(s)=CaO(s)+CO2(g)ΔH7CaO(s)+H2O(l)=Ca(OH)2(s)ΔH8
| A.① | B.④ | C.①②③ | D.②③④ |