为了探究硫酸铜对硫酸与锌反应速率的影响,有同学设计了在一定条件下进行如下实验,测量在不同试剂用量的反应条件下获得相同量气体所用的时间。
(1)请完成下表(填写表格中的空白处)(假设溶液混合时体积变化忽略不计)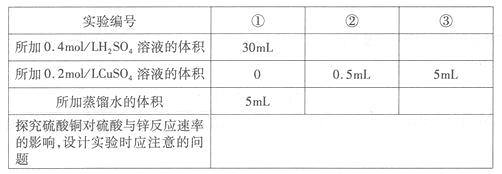
(2)实验③一段时间后可看到的锌粒表面呈 色。
(3)实验表明②号实验最快,③号实验最慢,可能的原因是
下图中的实验装置可以用于实验室制取乙炔。请填空:
(1)图中A管的作用是,
制取乙炔的化学反应方程式为。
(2)乙炔通入酸性KMnO4溶液中,发生反应,可以观察到
现象,若通入溴水中,发生反应。
(3)乙炔燃烧的化学方程式为,燃烧时的现象为,
为了安全,点燃乙炔前应该先。
现有四种试剂:
| A.新制Cu(OH)2悬浊液; | B.浓硝酸; | C.AgNO3溶液; | D.碘水。为了鉴别下列四瓶无色溶液,(其他实验条件略)请你选择合适的试剂,将其填入相应的括号中。 |
(1) 葡萄糖溶液() (2) 食盐溶液()
(3) 淀粉溶液() (4) 鸡蛋清溶液()
通常烷烃可以由相应的烯烃经催化加氢得到.但是,有一种烷烃A,分子式C9H20它却不能由任何C9H18的烯烃催化加氢得到.而另有A的三个同分异构体B1,B2,B3 却分别可由而且只能由一种自己相应的烯烃催化加氢得到.
试写出A,B1,B2,B3的结构简式。A是:;B1,B2,B3的结构简式是(没有顺序):
。
A、B、C、D是四种有机物,它们的分子中含有两个碳原子,其中A和B是烃。在标准状况下,A对氢气的相对密度是13,B与HCl反应生成C,C与D混合后加入NaOH并加热,可生成B。
(1)写出A、B、C、D的结构简式。A、B、C、D、
(2)写出有关化学方程式:、
。
下列各组物质中
1.丁烷和2—甲基丙烷 2.甲烷和丁烷 3.35Cl和37Cl 4.金刚石和石墨
(用序号填空)是同分异构体;是同素异形体;是同位素;是同系物。