盖斯定律认为能量总是守恒的:化学反应过程一步完成或分步完成,整个过程的热效应是相同的。
已知:①H2O(g)===H2O(l);ΔH=-Q1 kJ/mol;
②C2H5OH(g)===C2H5OH(l);ΔH=-Q2kJ/mol;
③C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g);ΔH=-Q3kJ/mol。
下列判断正确的是( )
| A.酒精的燃烧热为Q3kJ |
| B.若使23 g液体酒精完全燃烧,最后恢复到室温,释放出的热量为(1.5Q1-0.5Q2+0.5Q3)kJ |
| C.H2O(g)→H2O(l)释放出了热量,所以该过程为化学变化 |
| D.从反应③可知1mol C2H5OH(g)的能量高于2CO2(g)和3H2O(g)的总能量 |
(原创)化学与生产生活有密切的联系。以下说法正确的是
| A.埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
| B.气象环境报告中新增的“PM2.5”是对一种新分子的描述 |
| C.用浸泡过高锰酸钾溶液的硅藻土保鲜水果 |
| D.施肥时,草木灰(有效成分为K2CO3)与NH4Cl混合使用效果更好 |
在100mL密度为1.2g/mL稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有NO),向反应后溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀质量比原金属质量增加5.1g。则下列叙述不正确是
| A.当金属全部溶解时收集到NO气体的体积为2.24L(标准状况) |
| B.当生成沉淀的量最多时,消耗NaOH溶液体积最小为100mL |
| C.原稀硝酸的物质的量浓度一定为4 mol/L |
| D.参加反应金属总质量(m)为9.6g>m>3.6g |
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足下图所示转化关系的是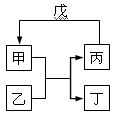
| 甲 |
乙 |
丙 |
戊 |
|
| ① |
NH3 |
O2 |
NO2 |
H2 |
| ② |
Fe |
H2O |
Fe3O4 |
Al |
| ③ |
Al2O3 |
NaOH溶液 |
NaAlO2溶液 |
过量CO2 |
| ④ |
Na2O2 |
CO2 |
O2 |
Na |
A.①③B.②③ C.②④ D.①④
下列电解质溶液的有关叙述正确的是
| A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH= 7 |
| B.在含有BaSO4沉淀的溶液中加人Na2SO4固体,c(Ba2+)增大 |
| C.含1molKOH的溶液与lmolCO2完全反应后,溶液中c(K+ ) =" c" (HCO3- ) |
| D.改变条件使醋酸溶液中的醋酸根离子浓度增大,溶液的pH值可能减小也可能增大 |
下列说法正确的是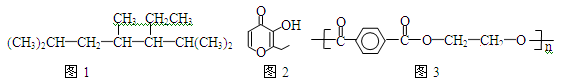
| A.按系统命名法命名时,(图1)化合物的名称是2,4,6-三甲基-5-乙基庚烷 |
| B.有机物(图2)的一种芳香族同分异构体能发生银镜反应 |
| C.高分子化合物(图3),其单体为对苯二甲酸和乙醇 |
| D.等质量的乙炔和苯完全燃烧生成水的质量相等 |