关于电解NaCl水溶液,下列叙述正确的是( )
| A.电解时在阳极得到氯气,在阴极得到金属钠 |
| B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕色 |
| C.若在阴极附近的溶液中滴入酚酞试液,溶液呈无色 |
| D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性 |
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法不正确的是
| A.原子半径的大小顺序为W>Q>Z>X>Y |
| B.元素X的气态氢化物与Q的单质可发生置换反应 |
| C.元素X与Y可以形成5种以上的化合物 |
| D.元素Q的最高价氧化物对应的水化物酸性比W的强 |
下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 |
结论 |
|
| A |
向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 |
HNO3分解生成了NO2 |
| B |
向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 |
淀粉没有水解成葡萄糖 |
| C |
向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 |
析出了NaHCO3 |
| D |
向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 |
使溶液褪色的气体是乙烯 |
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是
①1mol该有机物可消耗3molH2;②不能发生银镜反应;③分子式为C12H20O2;④它的同分异构体中可能有酚类;⑤1 mol该有机物水解时只能消耗1 mol NaOH
| A.②③④ | B.①④⑤ | C.①②③ | D.②③⑤ |
粒子甲与粒子乙在溶液中的转化关系如下图所示,粒子甲不可能是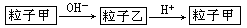
| A.NH4+ | B.Al | C.HCO3一 | D.SO2 |
下图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触,而稀硫酸又不够了。为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是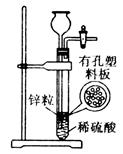
①食盐水②KNO3溶液③适量稀硫酸铜溶液
④醋酸钠溶液 ⑤苯 ⑥浓氨水
| A.①②④ |
| B.②⑤⑥ |
| C.③④⑤ |
| D.①③④ |