下列解释不科学的是
| A.“水滴石穿”主要是溶解了CO2的雨水与CaCO3长期作用下成了Ca(HCO3)2的缘故 |
| B.长期盛放NaOH溶液的滴瓶难打开,因为NaOH与瓶中的CO2反应形成“负压”的缘故 |
| C.“通风橱”是一种不负责任的尾气处理,因为实验产生的有害气体没有转化或吸收 |
| D.“雨后彩虹”、 “海市蜃楼”,既是一种自然现象又是光学现象,也与胶体有关 |
水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O32-+2H2O,下列说法正确的是
| A.x=2 | B.Fe2+、S2O32-都是还原剂 |
| C.硫元素被氧化,铁元素被还原 | D.每生成1 mol Fe3O4,则转移电子的物质的量为3 mol |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温下,10LpH=13的NaOH溶液中含有的OH-离子数为NA |
| C.标准状况下,11.2L己烷中含有分子的数目为0.5NA |
| D.100mL0.1mol·L-1的FeCl3溶液中含有Fe3+的个数为0.01 NA |
下列离子方程式书写正确是
| A.向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++HCO3—+OH-=CaCO3↓+H2O |
| B.将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-=2Fe2++S↓ |
| C.次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO |
| D.氯化亚铁溶液中加入稀硝酸:9Fe2++4H++NO3-=9Fe3++2H2O+NO↑ |
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
| 现象 |
解释 |
|
| A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
| B |
浓HNO3在光照条件下变黄 |
浓HNO3不稳定,生成棕色NO2能溶于浓硝酸 |
| C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
说明该溶液中含有SO42- |
| D |
向盐酸中加入浓硫酸时产生白雾 |
说明浓硫酸具有脱水性 |
用下列实验装置完成对应的实验(部分仪器巳省略),能达到实验目的的是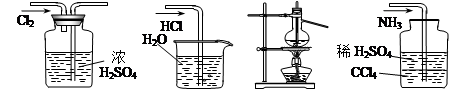
| A.干燥Cl2 | B.吸收HCl | C.液溴和苯的分馏 | D.吸收NH3 |