已知H2(g)+I2(g) 2HI(g);△H<0,有相同容积的密封容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入0.1mol H2和0.2molI2,相同温度下分别达到平衡。下列说法不正确的是
2HI(g);△H<0,有相同容积的密封容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入0.1mol H2和0.2molI2,相同温度下分别达到平衡。下列说法不正确的是
| A.乙中反应速率比甲中反应速率快 |
| B.平衡时甲、乙两容器中混合物的总物质的量之比为2︰3 |
| C.若平衡时甲中H2的转化率为40%,则乙中H2的转化率大于40% |
| D.平衡后,向乙中再加入0.1mol H2,建立新的平衡时,甲和乙中H2的百分含量不相同 |
某同学测得物质的量浓度均为0.01mol/LCH3COOH和CH3COONa混合溶液呈酸性后,得出了关系式,你认为其中不正确的是
| A.c(CH3COO—)>c(CH3COOH) |
| B.c(CH3CO0—)>c(Na+)>c(H+)>c(OH—) |
| C.c(Na+)=c(CH3COO—)=0.01mol/L |
| D.c(CH3COOH)+c(CH3COO—)=0.02mol/L |
下图是2004年批量生产的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2CH30H+302→2C02+4H20。下列说法正确的是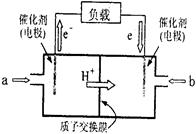
| A.左电极为电池的负极,a处通入的物质是甲醇 |
| B.右电极为电池的负极,b处通入的物质是空气 |
| C.负极反应式为:CH3OH+H20-6e-→CO2+6H+ |
| D.正极反应式为:02+2H20+4e-→40H— |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是
| 混合物 |
试剂 |
分离方法 |
|
| A |
苯(苯酚) |
溴水 |
过滤 |
| B |
甲烷(甲醛) |
银氨溶液 |
洗气 |
| C |
乙酸乙酯(乙酸) |
NaOH溶液 |
蒸馏 |
| D |
淀粉(氯化钠) |
蒸馏水 |
渗析 |
可逆反应aX(g)+b Y(g)  cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(u)一时间(t)图象如右图。则下列说法中正确的是
cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率(u)一时间(t)图象如右图。则下列说法中正确的是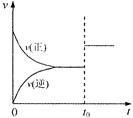
| A.若a+b=c,则t0时只能是增大了容器的压强 |
| B.若a+b=c,则t0时只能是加入了催化剂 |
| C.若a+b≠c,则t0时只能是增大了容器的压强 |
| D.若a+b≠c,则t0时只能是加入了催化剂 |
用NA表示阿伏加德罗常数,下列叙述中正确的是
| A.12g的金刚石晶体中含有碳碳键的数目为4NA |
| B.46g四氧化二氮含有的原子总数一定为3NA |
| C.500mLl.0mol/L的乙酸溶液中含有的H+数为0.5NA |
| D.1 molFeCl3制成胶体,所得胶体的粒子数为NA |