含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
回答下列问题:
(1)上述方案中,能测出Mg的质量分数的方案是 (填写代号,下同)
A.实验设计1 B.实验设计2 C.实验设计3 D.都可以
(2)上述方案中的化学反应体现了Mg、Al的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)某同学设计了右图装置。该装置适合的实验设计是 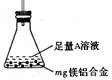

用该装置测定镁铝合金中镁的质量分数,所需的实验操作是
。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.称量反应前后,装置和药品的总质量
(4)若按实验设计3进行实验。将m g镁铝合金,溶于过量盐酸中,再加入过量的NaOH溶液,可得到白色沉淀,该沉淀物质是 (填化学式);将此沉淀洗净、干燥后,称得质量为w g。求合金中镁的质量分数 ;
(每空2分,共10分)
卤代烃分子里的卤原子与活泼金属阳离子结合,发生下列反应(X表示卤原子):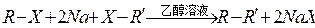

根据下图所示转化关系,完成下列填空: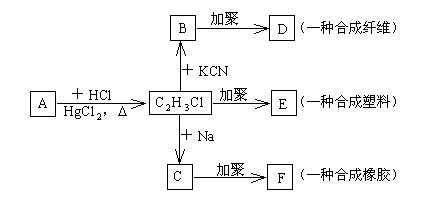
(1)A的分子式是,B的结构简式是,
E的结构简式是,
(2)B→D的化学方程式是。
(3)C→F的化学方程式是。
(每空1分,共10分)
已知化合物A中各元素的质量分数分别是C:37.5%,H:4.2%和O:58.3%,请填空:
(1)0.01mol A在空气中充分燃烧需消耗氧气1.01L(标准状况),则A的分子式是;
(2)实验表明:A不能发生银镜反应。1 mol A与足量的碳酸氢钠溶液反应可以放出3 mol CO2。在浓硫酸催化下,A与乙酸可发生酯化反应。核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境,则A的结构简式是;
(3)在浓硫酸催化和适宜的的反应条件下,A与足量的乙醇反应生成B(C12H20O7),B只有两种官能团,其数目比为3∶1,则由A生成B的反应类型是,该反应的化学方程式是;
(4)A失去1分子水后形成化合物C,写出C的两种可能的结构简式及其官能团的名称:①,,;
②,,。
实验室配置硫酸铝溶液时常滴入少量稀硫酸,解释:______。
在滴有酚酞的氨水中加入NH4Cl溶液后红色变浅,解释:______。
写出下列物质电离或盐水解的离子方程式:
(1)NaHSO4溶于水_______________________________________________________
(2) H2S的电离________________________________________________________
(3)氯化铁溶液:;
(4)碳酸钠溶液:;
(5)AlCl3与NaHCO3混合____________________________________________________