不能作为元素周期表中元素排列顺序的依据的是( )
| A.原子的核电荷数 | B.原子的核外电子数 | C.原子的质子数 | D.原子的中子数 |
物质分类是化学研究的重要方法之一,下列物质分类的正确组合是
| 混合物 |
碱 |
盐 |
碱性氧化物 |
酸性氧化物 |
|
| A |
液氧 |
苛性钠 |
胆矾 |
氧化铁 |
二氧化碳 |
| B |
盐酸 |
烧碱 |
食盐 |
氧化钠 |
一氧化碳 |
| C |
84消毒液 |
纯碱 |
石灰石 |
氨气 |
水 |
| D |
漂白粉 |
熟石灰 |
苏打 |
生石灰 |
二氧化硫 |
“纳米材料”是粒子直径为1~100 nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后会析出黑色沉淀
| A.①④⑤ | B.②③④ | C.②③⑤ | D.①③④⑥ |
下列对化学平衡移动的分析中,不正确的是
① 已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
② 已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大H2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大H2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③ 有气体参加的反应达平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④ 有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①③④ |
可逆反应a A(s)+b B(g) c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是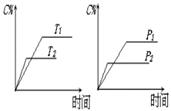
| A.达平衡后,加入催化剂则C%增大 |
| B.达平衡后,若升温,平衡左移 |
| C.化学方程式中b >c +d |
| D.达平衡后,增加A的量有利于平衡向右移动 |
强酸与强碱的稀溶液发生中和反应的热效应:
H+(aq)+OH-(aq)=H2O(1) △H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应△H1、△H2、△H3的关系正确的是
| A.△H1>△H2>△H3 | B.△H1<△H3<△H2 |
| C.△H1<△H2<△H3 | D.△H1>△H3>△H2 |