在恒温恒容的容器中进行反应A(g)?2B(g)+C(g),若反应物浓度由0.1mol·L-1降到0.06mol·L-1需20s,那么由0.06 mol·L-1降到0.024 mol·L-1,需要反应的时间是
| A.等于18s | B.等于12s | C.大于18s | D.小于18s |
工业上常用还原沉淀法处理含铬废水(Cr2O72—和CrO42—),其流程为:
已知:(1)步骤①中存在平衡:2Cr O42—(黄色)+2H+ Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
(2)步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH 一(aq)
Cr3+(aq)+3OH 一(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5 mol·L-1时可视作该离子不存在下列有关说法中,正确的是()
| A.步骤①中加酸,将溶液的pH 调节至2,溶液显黄色,CrO42—离子浓度增大 |
B.步骤①中当2v(CrO42 一)=v(Cr2O72—)时,说明反应2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O 达到平衡状态 Cr2O72—(橙色)+H2O 达到平衡状态 |
| C.步骤②中,若要还原1 mol Cr2O72一离子,需要12 mol(NH4)2Fe(SO4)2·6H2O。 |
| D.步骤③中,当将溶液的pH 调节至6 时,则可认为废水中的铬已除尽 |
根据右图,下列判断中正确的是
| A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
| B.烧杯b中发生反应为2Zn-4eˉ =2Zn2+ |
| C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极 |
| D.烧杯a中发生反应O2 + 4H++ 4eˉ = 2H2O,溶液pH降低 |
已知A、B为单质,C为化合物。
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C溶液中滴加过量NaOH溶液,先出现浑浊后澄清,则B可能为Al
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
能实现上述转化关系的是
A.①② B.②④ C.①③D.③④
下列情况下,离子组间一定能在溶液中同时大量共存的是
| A.pH=2的溶液中:SO42-、K+、NO3-、Mg2+ |
| B.pH试纸呈现红色的溶液:Fe2+、K+、NO3-、Na+ |
| C.水电离出的c(H+)=10-14mol/L的溶液中:Na+、HCO3-、Cl-、SO42- |
| D.CO32-可以大量存在的溶液:Ag+、K+、NO3-、Al3+ |
在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是 ( )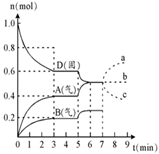
A.从反应开始到第一次达到平衡时,A物质的平均反应速率为0.0667mol/(L·min)
B.该反应的化学方程式为2D(s) 2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)
2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)
C.已知反应的△H>0,则第5分钟时图像呈现上述变化的原因可能是升高体系的温度
D.若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线