有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl
(1)属于离子化合物是___________;属于共价化合物是___________;
(2)只由离子键构成的物质是________;
(3)只由极性键构成的物质是________;只由非极性键构成的物质是________;
(4) 由极性键和非极性键构成的物质是______________;
(5) 由离子键和极性键构成的物质是_____________;
(6) 由离子键和非极性键构成的物质是________________。
(1)Na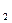 CO
CO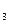 固体中混有少量NaHCO
固体中混有少量NaHCO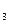 固体,除去的方法是_______,化学方程式为___________________。
固体,除去的方法是_______,化学方程式为___________________。
(2)NaHCO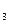 溶液中混有少量Na
溶液中混有少量Na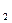 CO
CO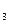 ,除去的方法是___________,反应的离子方程式为__________________________________。
,除去的方法是___________,反应的离子方程式为__________________________________。
(3)NaOH溶液中混有少量Na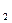 CO
CO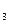 ,除去的方法是____________,反应的离子方程式为_________________________________。
,除去的方法是____________,反应的离子方程式为_________________________________。
(4)CO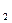 中混有少量的SO
中混有少量的SO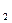 ,除去的方法是______________________,反应的化学方程式为_______________________________。
,除去的方法是______________________,反应的化学方程式为_______________________________。
下图中A至F是化合物,G是单质,它们之间有如下转化关系:
写出A、B、E、F的化学式。
A____________,B____________,E____________,F____________。
实验室临时需要用NaOH溶液和CO2来制取Na2CO3溶液。已知CO2气体在通入NaOH溶液时极易因其过量而生成NaHCO3,且无明显现象。实验室可供选择的试剂有:①未知浓度的NaOH溶液 ②37%盐酸 ③40%硫酸 ④14%盐酸 ⑤大理石 ⑥K2CO3固体 ⑦Cu2(OH)2CO3粉末
实验室现有如下仪器:铁架台,试管,量筒,烧杯,胶头滴管,单孔橡皮塞,玻璃导管,分液漏斗。
下表所列为有关物质在常温时的溶解度(g/100 g水):
| Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
| 15.9 |
8.40 |
35.8 |
35.5 |
20.0 |
40.0 |
(1)本实验应选用的仪器,除试管、胶头滴管、单孔橡皮管、玻璃导管外,还应有_____________。
(2)为了制取Na2CO3溶液,应选用合理的药品,除①外,还需要:___________________。
(3)为了制得只含Na2CO3溶质的溶液,请你设计一个实验方案(仪器安装不必叙述)_______________________________________________________________________________。
(4)根据给出的溶解度数据和上述实验方案,若保证在配制过程中不析出晶体,所用NaOH溶液中含NaOH溶质的质量分数的最大值是________________________________________。
1807年,英国化学家戴维在研究中发现:电解条件下可把水分解成H2和O2。他设想用电解的方法从KOH、NaOH中分离出K和Na。最初,戴维用饱和KOH溶液进行电解,不料还是得到H2和O2。这时,他考虑在__________条件下继续这项实验,不料,实验中产生的金属液珠一接触空气就立即燃烧起来,这时,他又考虑在__________条件继续实验,最后他终于成功地得到了银白色的金属钾。
A、B、C三种白色粉末,其焰色反应均为紫色,它们具有下列性质:
(1)均易溶于水,且A、B的溶液反应生成C的溶液。
(2)加热B的粉末时,生成无刺激性气味的气体D,D能使澄清的石灰水变浑浊,浑浊物为E。
(3)加热A、C时均不反应。
(4)少量C溶液通入过量D可以得到B。
(5)A溶液和D反应,A过量时生成C,A不足时生成B,则其化学式分别是:
A______________,B______________,C______________。
用离子方程式表示下列反应:
A+B___________________________________________________________。
D E______________________________________________________。
E______________________________________________________。
C+D___________________________________________________________。
A+D B____________________________________________________。
B____________________________________________________。
A+D C____________________________________________________。
C____________________________________________________。