人类的日常生产、生活都离不开水。
(1)化学课上同学们分组研究水的净化及组成(装置如图)。其中一组同学用自制简易净水器(图②所示)净化池塘水,其中活性炭的作用是 ,净化后的池塘水与矿泉水、蒸馏水、自来水四种水中属于纯净物的是_________。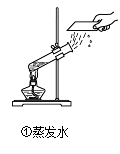


(2)实验③中通电一段时间后,试管b中气体的气体是 (填写化学式),该
实验说明水是由 组成的,反应的化学方程式为 。
(3)请根据电解水的微观示意图分析:由于化学反应前后原子的 、 和质量都没有发生变化,因此在化学反应中质量守恒。 
(4)从微观角度分析,实验①和③两个变化中最本质的区别是 。
(4分) 小丽配制50.0 g 15.0%的氯化钾溶液的操作步骤为:
(1)计算:需要氯化钾固体的质量为g。
(2)称量:用托盘天平称取所需固体。若所用砝码生锈了,则会导致氯化钠溶液的溶质质量分数(填“<”或“>”)15.0%。
(3)溶解:该操作中用(填仪器名称)搅拌至完全溶解。
(4)装瓶:将配制的溶液倒入(填“广口瓶”或“细口瓶”),并贴上标签。
请仔细观察右图,回答有关问题: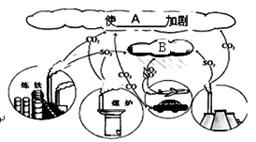
(1)图中A所代表的一个名词是。
(2)要缓解图中B所反映的环境问题,请你提一条合理化建议。
请从下列物质中选择适当的物质填空(填序号):
| A.干冰 | B.盐酸 | C.煤 | D.石油 |
E.小苏打F.硝酸钾 G.葡萄糖 H.烧碱
(1)能被人体直接吸收的营养物质是;(2)可用于人工降雨的物质是;
(3)常用于铁制品表面除锈的是;(4)被誉为“工业的血液”的是;
(5)农田施用的复合肥是;(6)常用于治疗胃酸过多的是。
用化学用语填空:
(1)2个钠离子;(2)地壳中含量最多的金属元素的氧化物;
(3)最简单的有机物;(4)硫酸锌中锌元素的化合价。
民以食为天。粮食是当今世界面临的五大问题之一。请根据所学知识回答下列问题:
(1)好种出好苗“为了选种子,需配制15%的食盐溶液。现要配制100Kg15%的食盐溶液需水Kg。配制食盐溶液的一般步骤为:④贴标签。
(2)庄稼一枝花,全靠肥当家。某班同学就施用化肥的“利”与“弊”为题进行辩论,正方观点是施用化肥有利,正方下列观点中不科学的是()
| A.化肥肥效快 |
| B.化肥可使农作物增产 |
| C.复合肥料能给作物提供多种营养元素 |
| D.化肥成分单一,长久使用不会破坏土壤结构 |