已知某种铸造钢轨的金属粉末原料中可能含有铁、锰、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究。
(1)提出猜想:
猜想一:该粉末由铜、锰组成; 猜想二:该粉末由铁、锰组成;
猜想三:该粉末由铁、锰、铜组成; 猜想四:该粉末由 组成。
(2)查阅资料:金属锰不能被磁铁所吸引,锰和FeSO4溶液可以发生置换反应,Mn元素在生成物中显+2价,生成物的溶液为浅粉色。
(3)进行实验:
| 实验目的 |
实验操作 |
实验现象 |
| ①证明粉末中是否含有铜 |
取一个小烧杯,加入适量的粉末,再向其中加入足量的 。 |
有少量红色粉末不能溶解。 |
| ②证明粉末中是否含有 |
取5.5克粉末放入烧杯,再向其中加入适量的硫酸亚铁溶液,反应完全后过滤、干燥,称量固体为5.52克。 |
。 |
| ③证明粉末中是否含有铁 |
另取5.5克粉末, (用物理方法), 称量剩余金属粉末为1.12克。 |
。 |
(4)初步结论:猜想___________成立;实验①中发生反应的化学方程式为___________。
(5)数据处理:试计算粉末原料中任意一种金属所占的质量分数(用金属名称和百分数表示,结果保留一位小数)_______________________________。
某化学兴趣小组的同学按照课本上的实验装置做“测定空气中氧气的体积分数”实验(如图所示),但测出的氧气的体积分数明显小于1/5。请你参与探究: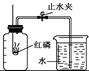
(1)提出问题:造成误差的原因是什么?如何改进课本上的实验装置?
(2)查阅资料:红磷、白磷的一些性质如下表:
| 颜色、状态 |
熔点/℃ |
着火点/℃ |
密度/(g/cm3) |
|
| 红磷 |
暗红色固体 |
590 |
240 |
2.34 |
| 白磷 |
白色或黄色固体 |
44.1 |
40 |
1.82 |
(3)猜想与假设:
①甲同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性。
②乙同学:可能是瓶内残留气体中还有氧气。
③你还能作出的猜想是。
(4)交流与讨论:
①丙同学认为用木炭代替红磷,就可以消除误差,你认为他的猜想,(填“合理”或“不合理”)理由是。
②他们对课本上的实验装置进行了图2所示的改进(其他仪器忽略)。
a.甲同学提出应把红磷换为白磷,理由是_______________。
b.通过粗铜丝来点燃玻璃管内的白磷,这利用了金属的性。
c.与课本上的实验装置相比较,该装置的一个优点是_________________________________.
(5)探究与反思:
①为了验证乙同学的猜想,将铜粉放在残余气体中加热,观察到铜粉变黑色,证明乙同学的猜想(填“合理”或“不合理”)
②大家用改进的实验装置(如图所示)进行实验,待玻璃管冷却、管内白色的烟幕消失时,左玻璃管内的液面上升了1格,得到了较准确的结果,但又意外发现左玻璃管内壁上端附着黄色固体。左玻璃管上端的黄色固体的主要成分可能是。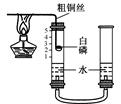
小明同学在一本化学资料中发现KClO3晶体在MnO2的催化下,能分解生成O2和氯化钾,于是提出疑问,CuO能催化KClO3的受热分解反应吗?于是设计了以下实验:
[实验方案] ①任取2份氯酸钾,分别放于两支试管中,仅向其中一支试管中加入m克CuO; ②将上述盛有KClO3的两支试管,在相同条件下同时加热,并使产生的气体通入水中,观察产生气泡的速率 , 比较产生气体的速率;③充分反应后冷却,将放入CuO的试管内固体残余物加水溶解,滤出不溶物,洗涤并干燥; ④观察滤出固体物质的颜色状态为黑色固体。 ⑤将滤出固体与碳粉混合后,在密闭容器中加热,将所产生的气体通过澄清石灰水,观察现象黑色固体变为红色,石灰水变浑浊 。
[交流讨论] (1)步骤:①②的目的是通过对比实验,探究
在第三步过滤操作中用到的玻璃仪器为、 、
(3)步骤⑤的目的是证明
(4)小红认为小明实验中有缺陷,请你帮小红改进实验中的不足之处: 、
下图所示为实验室常用的实验装置: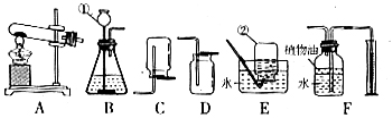
据此回答下列问题:(1)写出带标号仪器的名称:
①②
常温下,用锌和稀硫酸反应制取氢气,应选用的发生装置是
(填序号,下同),收集装置是
(3)实验室通常用稀盐酸和石灰石反应制取CO2,该反应的化学方程式为,检验CO2的化学方程式此外CO2也可以用碳酸氢钠(NaHCO3)固体加热分解(产物为碳酸钠、二氧化碳和水)来制取,该反应的化学方程式为若用此法来制取CO2,应选用的发生装置是,收集装置是
(4)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是,植物油上方原有的空气对实验的结果(填“有”或“没有”)明显影响。
某同学为了研究竹子里面气体的成分,做了一个实验:
(1)他先将竹子浸在水里,钻一小孔,看到一串串气泡冒出,然后采用法收集到了甲乙两瓶气体;
(2)将放有足量红磷的燃烧匙伸入甲瓶中(如图)。用放大镜聚焦,使红磷燃烧,瓶内充满了白烟。然后,将该瓶倒放水中,松开夹子,结果流入的水约占瓶子容积的1/10,说明竹子里气体中肯定含有。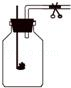
(3)再往乙瓶中倒入一些澄清石灰水,发现石灰水马上变浑浊,说明竹子气体里肯定有。
(4)那么竹子里的气体含量与空气有什么区别呢?于是,他又用空气重做了上述两个实验.相比较后得出的结论是。
小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 实验序号 |
KClO3质量 |
其他物质质量 |
待测数据 |
| ① |
1.2g |
/ |
|
| ② |
1.2g |
CuO0.5g |
|
| ③ |
1.2g |
MnO2 0.5g |
(1)上述实验应测量的“待测数据"是;
(2)若实验②比实验①的“待测数据”更_______(选填“大"或“小"),说明氧化铜能加快氯酸钾的分解速率;
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,再将该黑色粉末放入试管中,加入________________,若观察到,说明黑色粉末的化学性质在反应前后保持不变。
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是___________