向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是( )
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
| C.该实验不能证明[Cu(NH3)4]2+比氢氧化铜稳定 |
| D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
元素“氦、铷、铯”等是用下列哪种科学方法发现的:
| A.红外光谱 | B.质谱 | C.原子光谱 | D.核磁共振谱 |
已知甲、乙、丙三种物质均含有同一种短周期元素,其中甲为单质,其转化关系如下: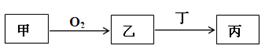
下列说法不正确的( )
| A.若丙既具有漂白性又具有氧化性,则丁可能是Cl2 |
| B.若甲是某种金属,则丁可能是盐酸,也可能是氢氧化钠溶液 |
| C.若甲是某种非金属,且甲和丙反应可以生成乙,则丁可能是Fe |
| D.若甲是某种非金属,则丙可能是一种用于制备防火材料的物质 |
用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S
下列说法正确的是( )
| A.反应中硫元素被氧化,所有铁元素均被还原 |
| B.还原剂是S2-和Cu+,氧化剂是Fe3+ |
| C.氧化产物是S,还原产物是Cu2+和Fe2+ |
| D.当转移1 mol e-时,有46 g CuFeS2参加反应 |
如图所示,6个编号分别代表下列物质中的一种物质, 凡是用直线相连的两种物质均能发生化学反应(已知高温下氨能还原氧化铁):
a. Al b.Fe2O3c.NaOH溶液d. HI溶液 e.NH3 f.Cl2
图中⑤表示的物质是( )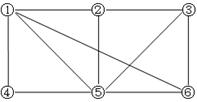
| A.a或b | B.c | C.d | D.e或f |
25℃时,已知弱酸的电离常数:K(CH3COOH)=1.8×10-5;K1(H2CO3)=4.4×10-7;K2(H2CO3)=4.7×10-11;K(HClO)=4.0×10-8。则下列说法正确的是( )
| A.25℃时,0.1mol/L的醋酸溶液比0.01mol/L的醋酸溶液的K值小 |
| B.25℃时,甲基橙滴入0.1mol/L的醋酸溶液中,溶液呈黄色 |
| C.新制氯水与碳酸氢钠不反应 |
| D.等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH:pH[Na2CO3(aq)]>pH[NaClO(aq)]>pH[CH3COONa(aq)] |