下列实验方法、结论合理的是
| A.增加反应物的用量,化学反应速率一定加快 |
| B.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 |
| C.pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强 |
| D.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为碳酸钠 |
下列有关说法中,正确的是
| A.苯和乙烯都可以使溴的四氯化碳溶液褪色 |
| B.等物质的量的乙烯和乙醇完全燃烧消耗氧气的量不相等 |
| C.乙醇的酯化反应和酯的水解反应均属于取代反应 |
| D.聚乙烯可以发生加成反应 |
下列实验装置设计正确且能达到目的的是
| A.实验I:静置一段时间,小试管内有晶体析出 |
| B.实验II:制取氧气 |
| C.实验III除CO2气体中的HCL |
| D.实验IV:配制一定物质的量浓度的稀硫酸 |
对下列化学用语描述和理解都正确的是
A.原子结构示意图 ,可以表示 ,可以表示 ,也表示 ,也表示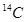 |
B.比例模型 可以表示水分子,也可以表示二氧化碳分子 可以表示水分子,也可以表示二氧化碳分子 |
C.结构示意图为 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 |
D.电子式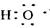 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
化学与生活密切相关,下列说法正确的是:
| A.制作航天服的聚酯纤维属于新型无机非金属材料 |
| B.银器久置后表面会变暗,是因为发生了电化学腐蚀 |
| C.Li是最轻的金属也是活动性很强的金属,是制造电池的理想物质 |
| D.海水提取溴、煤的液化、焰色反应都发生了化学变化。 |
下列操作不能达到实验目的的是
| 选项 |
实 验 目 的 |
实 验 操作 |
| A |
在溶液中将MnO4—完全转化为Mn2+ |
向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| B |
验证Br2的氧化性强于I2 |
将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| C |
检验Fe(NO3)2晶体是否已氧化变质 |
将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| D |
验证Fe(OH)3的溶解度小于Mg(OH)2 |
将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |