(12分〉某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀。查阅资料得知常温下BaSO3的KSP为 ,饱和亚硫酸中
,饱和亚硫酸中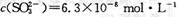 。
。
(1) 将0.1 mol • L—1的BaCl2溶液滴入饱和亚硫酸中,_______ (填“能”或“不能”)生成BaSO3沉淀,原因是______________ (请写出必要的推断过程)。
(2) 浓硫酸的沸点为338°C,酒精灯火焰的温度为400〜5000C,甲同学用装置I进行实验,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸。
①写出加热试管中发生反应的化学方程式:_____________________
②白色沉淀的化学式是_______,请用离子方程式表示生成该白色沉淀的可能原因___________________________________
(3) 乙同学认为甲同学的装置不完善,设计了改进装置II进行实验(夹持装置和A中加热装置已略,气密性已检验)。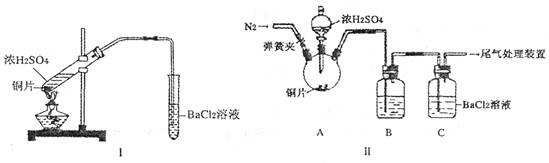
①打开弹簧夹,通入N2—段时间后关闭弹簧夹
②滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成。
操作①的目的是_______,洗气瓶B中的试剂是______________。
(4) 丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,也产生不溶于盐酸的白色沉淀,丙滴加的试剂可能是______________。
| A.NaOH溶液 | B.Na[Al(OH)4]溶液 | C.H2O2溶液 | D.酸性 KMnO4溶液 |
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。
某化学研究小组采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5,装置II中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2→Na2S2O5
(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,需要用到的玻璃仪器有 。
装置III用于处理尾气,可选用的合理装置(夹持仪器已略去)为 (填序号)。
现将0.5mol Na2S2O5溶解于水配成1L溶液,该溶液pH=4.5。溶液中部分微粒浓度随溶液酸碱性变化如图。
(3)写出Na2S2O5溶解于水的化学方程式 ;
当溶液pH小于1后,溶液中H2SO3的浓度减小,其原因可能是 。
(4)葡萄酒常用Na2S2O5做抗氧化剂。1.90g Na2S2O5最多能还原 mLO2(标准状况)。
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是 。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放出25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至终点,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶中加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)滴定终点时的现象为锥形瓶中的溶液_________________________;
(2)该小组在步骤①中的错误是_______________,由此造成的测定结果__________(填“偏高”或“偏低”或“无影响”);
(3)如上图是某次滴定时的滴定管中的液面,其读数为_______mL;
(4)根据下列数据:
| 测定次数 |
待测液体积/mL |
标准盐酸体积/mL |
|
| 滴定前读数/mL |
滴定后读数/mL |
||
| 第一次 |
25.00 |
0.40 |
20.38 |
| 第二次 |
25.00 |
4.00 |
24.02 |
计算得出待测烧碱溶液的物质的量浓度为_____________。
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图。
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大,I2(S) + I- I3-(aq)。
I3-(aq)。
容器中盛放的试剂分别为:
A.MnO2
C.0.5000 mol/L的KI溶液
D.AgNO3溶液
E.NaOH溶液
F.浓盐酸
完成下列填空:
(1)仪器A的名称 ,B中的试剂是_________________。
(2)当D装置中出现 时,停止加热;E的作用是_______________。
(3)当氯气开始进入C时,C中看到的现象是____________________;不断向C中通入氯气,看到溶液颜色逐渐加深,后来出现深褐色沉淀,试运用平衡移动原理分析产生这些现象的原因___________________。
(4)持续不断地向C中通入氯气,看到C中液体逐渐澄清,最终呈无色。推测此时C中无色溶液里含碘物质的化学式_________________(此时溶液中只有一种含碘微粒)。
为确定含碘物质中碘元素的化合价,进行如下实验:
① 取反应后C中溶液5.00mL(均匀)于锥形瓶中,加入KI(过量)和足量稀硫酸。
②向上述锥形瓶中滴加淀粉指示剂,溶液变蓝,用0.6250 mol/L的Na2S2O3溶液滴定至蓝色刚好褪去,耗Na2S2O3溶液24.00 mL。
已知: I2 + 2 S2O32-→ 2 I-+ S4O62-
计算:碘元素的化合价为_______________。
(5)欲检验某溶液中是否含有I-,可使用的试剂为氯水和淀粉溶液。合理的实验操作为_________________________________。
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
(1)写出装置A发生反应的离子方程式 。
若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是
(2)①装置B中盛放的试剂名称为 ,现象是 。
②装置D和E中出现的不同现象说明的问题是 。
③装置F的作用是 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),装置中应放入 (填写试剂或用品名称)。
某探究小组用酸性KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。实验条件作如下限定:催化剂的用量可选择0.5g、0g,酸性KMnO4溶液的浓度可选择0.01mol·L﹣1、0.001mol·L﹣1,实验温度可选择298K、323K.每次实验KMnO4酸性溶液的用量均为4 mL,H2C2O4溶液(0.1mol·L﹣1 )的用量均为2mL。
(1)该反应的离子方程式: 。
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 |
T/K |
催化剂的用量/g |
KMnO4酸性溶液的浓度/mol·L﹣1 |
实验目的 |
| ① |
298 |
0.5 |
0.01 |
(Ⅰ )实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; (Ⅱ )实验①和③探究温度对该反应速率的影响; (Ⅲ )实验①和 探究催化剂对该反应速率的影响 |
| ② |
||||
| ③ |
||||
| ④ |
(3)在完成探究催化剂对该反应速率影响的实验时发现,未加催化剂的情况下,刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。针对上述实验现象,同学认为高锰酸钾与草酸溶液的反应放热,导致溶液温度升高,反应速率加快,从影响化学反应速率的因素看,你猜想还可能是 。若用实验证明你的猜想.除酸性高锰酸钾溶液,草酸溶液外,还需要选择的试剂最合理的是 。
A.硫酸钾 B.硫酸锰 C.二氧化锰 D.水
(4)可以利用酸性高锰酸钾测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数,该小组称量2.68 g草酸钠样品溶于稀硫酸中,然后用0.2000 mol·L﹣1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应 )。
①滴定前是否要滴加指示剂? (填“是”或“否” ),当溶液 ,说明滴定达到终点。
②滴定时用 (填a或b )滴定管盛装KMnO4标准溶液。
③达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。