HNCO可用于消除汽车尾气中的NO和NO2,其反应原理为: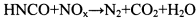 下列说法正确的是()
下列说法正确的是()
| A.HNCO分子中存在非极性键 | B.4.3g HNCO中含有0.1 NA个原子 |
| C.反应中NOx还原剂 | D.1mol NO2在反应中转移4NA个电子 |
下列溶液中NO3-的物质的量浓度最大的是
| A.500 mL 1 mol·L-1的KNO3溶液 |
| B.500 mL 1 mol·L-1的Ba(NO3)2溶液 |
| C.1000 mL 0.5 mol·L-1的Mg(NO3)2溶液 |
| D.1 L 0.5 mol·L-1的Fe(NO3)3溶液 |
下列反应不属于四种基本反应类型,但属于氧化还原反应的是
| A.Fe+CuSO4=FeSO4+Cu |
B.Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
| C.AgNO3+NaCl=AgCl↓+NaNO3 |
D.2KMnO4 K2MnO4 +MnO2 +O2↑ K2MnO4 +MnO2 +O2↑ |
某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是
| A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成 |
| B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成 |
| C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
下列关于电解质溶液的正确判断是
| A.在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存 |
| B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存 |
| C.由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH- |
D.由0.1 mol·L-1一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H2O HA+OH- HA+OH- |
下列叙述正确的是
| A.95 ℃纯水的pH<7,说明加热可导致水呈酸性 |
| B.pH=3的醋酸溶液,稀释至10倍后pH=4 |
| C.0.2 mol·L-1的盐酸,与等体积水混合后pH=1 |
| D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7 |