Y 元素最高正价与负价的绝对值之差是4;Y元素与M 元素形成化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
| A.KCl | B.Na2S | C.Na2O | D.K2S |
下列叙述正确的是( )
| A.离子晶体中,只存在离子键,不可能存在其它化学键 |
| B.氧族元素(O、S、Se、Te)的氢化物的沸点依次升高 |
| C.NaHSO4、Na2O2晶体中的阴阳离子个数比均为1∶1 |
| D.晶体的硬度:金刚石>碳化硅>石英 |
下列说法正确的是( )
| A.由于铵盐是由离子键构成的,因而化学性质相当稳定 |
| B.分子晶体中都存在分子间作用力,但可能不存在共价键 |
| C.在常见的四种晶体类型中,都有“原子(离子)半径越大,物质熔点越低”的规律 |
| D.常温下为气态或液态的物质,其固态时一定会形成分子晶体 |
近年来,科学家合成一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150 ℃,燃烧热极高。下列说法肯定错误的是( )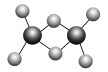
| A.Al2H6在固态时所形成的晶体是分子晶体 |
| B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
| D.氢铝化合物中可能存在组成为AlnH2n+2的一系列物质(n为正整数) |
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如下图)。下列有关说法正确的是 ( )
| A.正硼酸晶体属于原子晶体 |
| B.H3BO3分子的稳定性与氢键有关 |
| C.分子中硼原子最外层为8电子稳定结构 |
| D.含1 mol H3BO3的晶体中有3 mol氢键 |
下列图像是NaCl、CsCl、ZnS等离子晶体结构图或是从其中分割出来的部分结构图。试判断属于NaCl的晶体结构的图像为 ( )