在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变压强时,颜色也会改变,但平衡并不移动,这个反应是( )
A.2NO+O2  2NO2 2NO2 |
B.N2O4 2NO2 2NO2 |
C.Br2(g)+H2 2HBr 2HBr |
D.6NO+4NH3 5N2+3H2O 5N2+3H2O |
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
| 选项化合物 |
A |
B |
C |
D |
| Y |
CO2 |
Fe2O3 |
C2H5OH |
FeC l3 l3 |
| W |
MgO |
Al2O3 |
C2H5ONa |
CuCl2 |
某无色溶液中可能含有Na+、K+、Fe3+、NH4+、Cu2+、SO42-、SO32-、CO32-、Cl-、
Br-这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:
①pH试纸检验,溶液的pH>7。
②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。
③另取少量原溶液,向溶液中滴加足量氯水,无气体产生,再加入CCl4振荡,静置后CCl4层呈橙色,用分液漏斗分液。
④向 分液后的水溶液中加入Ba(NO3)2溶液和HNO3溶液,有白色沉淀产生,过滤。
分液后的水溶液中加入Ba(NO3)2溶液和HNO3溶液,有白色沉淀产生,过滤。
⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生。
则关于原溶液的判断中不正确的是
| A.肯定存在的离子是Na+、K+、SO32-、Br- |
| B.肯定不存在的离子是Fe3+、Cu2+、NH4+、SO42-、CO32- |
| C.无法确定原溶液中是否存在Cl- |
| D.若步骤④改用BaCl2溶液和盐酸的混合溶液,则对溶液中离子的判断无影响 |
下图所示对实验仪器名称的标注或实验操作正确的是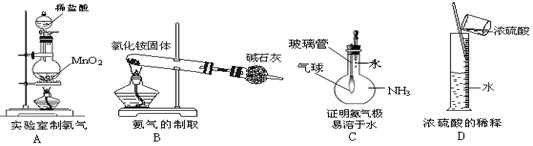
下列用来表示物质变化的化学反应中.正确的是
| A.表示中和热的热化学方程式:H++OH— |
| B.硫酸氢铵溶液与少量氢氧化钠溶液混合共热的离子方程式:NH4++OH— |
C.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式: 3ClO— + 2Fe(OH)3 +4H+ +4H+ |
| D.高锰酸钾酸性溶液与双氧水反应的离子方程式:2MnO4—十5H2l8O2+6H+ |
下列离子方程式书写不正确的是
| A.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+4I-=2I2+2H2O |
B.硫化钠的水解反应:S2-+H2O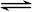 HS-+OH- HS-+OH- |
| C.4mol/L的KAl(SO4)2溶液与7mol/L的Ba(OH)2溶液等体积混合: 4Al3++7SO42—+7Ba2++14OH—=2Al(OH)3↓+2AlO2—+7BaSO4↓+4H2O |
| D.硝酸银溶液中滴加过量氨水:Ag++NH3·H2O=AgOH↓+NH4+ |