一定条件下向容积为20 L的密闭容器中充入1 mol NO2气体,发生反应2NO2  N2O4。反应中测得相关数据如下表所示:
N2O4。反应中测得相关数据如下表所示:
| 反应时间/min |
0 |
10 |
20 |
30 |
40 |
50 |
| 气体相对分子质量 |
46 |
57 |
64 |
69 |
69 |
69 |
(1)此条件下该反应的化学平衡常数Kc=________。(填表达式)
(2)在50 min末,向容器中加入 mol NO2,若要保持平衡不发生移动,则应加入N2O4________mol。
(3)若保持容器体积不发生变化,升高温度,则可得如图图像,据此判断该反应ΔH________0(填“大于”、“小于”或“等于”)。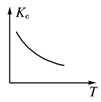
(4)若在体积不变的情况下,开始充入0.5 mol N2O4,则达到新平衡时N2O4的转化率α=________。
分子式为C4H10O的有机化合物A。按要求完成下列问题:(每空1分,共5分)
(1)若A能在催化剂作用下连续氧化生成羧酸,请写出它可能的结构简式为、。
(2)当C原子与4个不同的原子或基团相连时该碳原子称作“手性”碳原子。则分子式为C4H10O的有机化合物中,含有“手性”碳原子的结构简式为________________。
(3)A(C4H10O) B(C4H8),已知:A分子中有三个甲基。A与浓HBr溶液一起共热生成H
B(C4H8),已知:A分子中有三个甲基。A与浓HBr溶液一起共热生成H
写出A、H的结构简式、
按要求完成下列问题(方程式2分,其余每空1分,共13分)
(1)用系统命名法命名下列有机物
① ;
;
②
③(CH3)3CCH2OH
④4―甲基―1―戊烯的结构简式为 。
(2)现有四种有机物:
| A.(CH3)2CHCl | B.CH3CH2OOCH |
| C.OHCCH2COOH | D.CH3COOCH2 |
①在一定条件下能与新制Cu(OH)2反应的有
②能与NaOH水溶液反应的有
(3)写出乙醛与含过量氢氧化钠溶液的新制氢氧化铜反应的化学方程式
(4)选择适当的试剂以实现下列转变,将化学式填在横线上
①②③④⑤
将1.92 g铜置入一定量的浓硝酸中,并微热,随着铜的不断减少,反应生成的气体颜色逐渐变浅,当铜反应完毕时(铜片完全消失),共收集到标况下气体1.12 L(设不含N2O4),求:
(1)收集到的气体中主要有含有;
(2)上述过程中,有关反应的化学方程式为;;
(3)反应中被还原的HNO3的物质的量是;
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2,使其充分反应,若要使水恰好充满容器,理论上需要参加反应的O2的物质的量是多少摩尔?(计算过程)
化学兴趣小组为探究某铁矿石(主要成分为Fe2O3和SiO2)的性质,进行如下实验: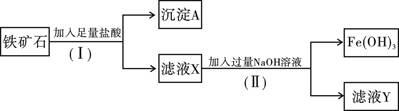
(1)步骤(I)中分离溶液和沉淀的操作名称是;
(2)沉淀A中一定含有,该物质属于氧化物;(填“酸性”或“碱性”)
(3)要检验滤液X中的金属阳离子,应加入;
(4)写出步骤(Ⅱ)中生成Fe(OH)3的离子方程式;
(5)溶液Y中溶质的化学式为 。
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
(1)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示该物质C的一个重要应用;
(2)若A是一种黄色单质固体,则B→C的化学方程式为;
(3)若A是一种黑色非金属单质固体,写出B的一个用途;
(4)若C是红棕色气体,则A化学式可能为,试写出C与水反应的化学方程式。