某同学使用下图5-1所示装置,试验一氧化碳与氧化铁的反应。
请回答下列有关问题:
(1)该实验的目的是 。
(2)有下列实验步骤:①加热;②通人一氧化碳,请用上述实验步骤的标号填空。实验开始时,应先 ;然后 。发生反应的化学方程式为 。
(3)实验进行一段时间后,A装置中出现的现象为 ;说明有 生成。
B装置中出现的现象为 说明有 生成。
右图有多种功能,如收集气体、洗涤气体、贮存气体等。回答下列问题: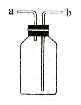
(1)气体从a端进入集气,该气体必须具有的性质是。
(2)气体从b端进入集气,该气体必须具有的性质是。
(3)将此装置倒置后,气体从a端进入集气,该气体必须具有的性质是。
(4)将此装置倒置后,气体从b端进入集气,该气体必须具有的性质是。
(5)装置中预先盛满水,将水排出贮气,气体从端进入。
(6)用水将瓶中贮有的气体排出使用,水从端进入。
下列事实说明空气中含有哪些成分?
(1)小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有___________;
(2)空气是制造氮肥的主要原料说明空气中含有____________;
(3)酥脆的饼干在空气中放置会逐渐变软说明空气中含有____________;
(4)长期放置在空气中的石灰水表面有一层白色物质说明空气中含有____________。
根据右图几种粒子的结构示意图,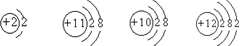
①②③④
回答问题:
⑴其中属于阳离子的是(填序号,下同)。
⑵具有相似化学性质的元素是。
在日常生活中应注意合理摄取营养物质和人体必需的元素。
(1)蛋白质是构成生命的基础物质,是日常膳食的重要组成部分。下列食物:①苹果②葡萄干③牛奶④米饭
其中含有丰富蛋白质的是 (填写编号)。
(2)人体摄入的淀粉在酶的催化作用下与水作用最终变成葡萄糖,葡萄糖在酶的催化作用下经缓慢氧化转变成水和,同时放出能量,供机体活动和维持恒定体温的需要。
甲、乙、丙三种物质的溶解度曲线如右图所示。据图回答: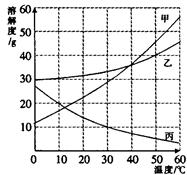
(1)50℃时,乙物质的溶解度是g;
(2) 在不改变溶液质量的情况下,要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是:;
(3) 50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是,所得溶液中溶质质量分数最小的是。