下图是配制50g质量分数为5% 的氯化钠溶液的操作过程示意图: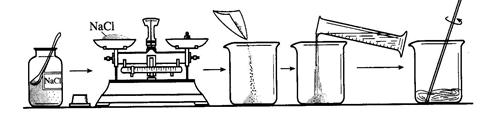
A B C D E
试回答:
(1)B操作中应称量氯化钠的质量是 g 。放好砝码和游码后,向托盘上加氯化钠时,若指针偏向分度盘的左边,应进行的操作是
。
(2)D操作应选用 mL 的量筒(从10 mL、100 mL中选择);量水时,量筒必须平放,视线要跟量筒凹液面的 处保持水平。
(3)E操作的作用是 。
实验室用如图所示装置制取氧气,下列实验操作正确的是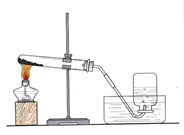
| A.加热前,将集气瓶注满水,用玻璃片盖着倒立在盛水的水槽中 |
| B.先将导管口移入集气瓶,再开始加热 |
| C.收集O2后,将集气瓶移出水槽,然后盖上玻璃片 |
| D.停止加热时,先熄灭酒精灯,再移出导气管 |
现有CO、CO2、H2、水蒸气四种气体组成的混合气体,按如下图装置进行实验。(已知:无水硫酸铜遇水变蓝色)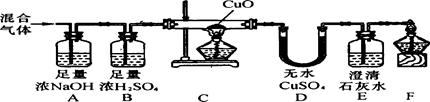
(1)若只验证混合气体中的CO和H2, 请回答:
①使用装置A的目的是,其中发生的化学方程式是
②使用装置B的目的是。
③若A、B装置顺序对调,造成的后果是。
④若A、E装置顺序对调,造成的后果是。
⑤F装置的作用是。
(2)学习中编顺口溜或打油诗,是帮助记忆的好方法。现有如下打油诗:
水晶宫中卧包公,阵阵清风吹进宫;
忽有烈火烧过来,竟把包公变关公;
烈火退去清风在,吹得关公好轻松。
根据这首打油诗的描述,你认为这首打油诗描写的实验可能是
①一氧化碳还原氧化铜②氧气和铜的反应
③氢气还原氧化铜④木炭还原二氧化碳
(3)某混合气体中可能含有氢气、一氧化碳、二氧化碳的一种或几种。把混合气体通入灼热的盛有足量氧化铜的试管(已排尽空气),充分反应后,管内固体物质质量减少1.6克,将反应完全后的气体全部通入过量的澄清石灰水,充分反应后,得到10克白色沉淀,则混合气体的组成可能的是。
A.一氧化碳 B.氢气和二氧化碳
C.一氧化碳、氢气D.氢气、一氧化碳、二氧化碳
我市在“三创”期间对大量盆栽鲜花施用了S一诱抗素制剂,以保证鲜花盛开。已知S-诱抗素分子的化学式为C15H20O4请回答:
(1)s-诱抗素中碳、氢、氧三种元素的原子个数比为 。
(2)S一诱抗素的相对分子质量为。
(3)S一诱抗素中氧元素的质量分数为。
(共8分)根据下列实验装置图,回答问题:
(1)写出标有序号的仪器名称:①_____________,②____________;
(2)在实验室中用过氧化氢溶液和二氧化锰混合制取氧气时,其中二氧化锰起______作用,发生反应的化学方程式为_____________________________________________;
(3)实验室制取二氧化碳气体,应选择的发生装置为_________(填写装置的字母代号,下同);应选用的收集装置是___________。检验二氧化碳是否收集满的方法是:将燃着的木条放在__________________,观察火焰是否熄灭。
(共7分)钢铁是重要的金属材料,在生产、生活中有广泛的用途。我市建造的国际会展中心使用了大量的钢铁。
(1)钢铁属于______________(填“纯净物”或“混合物”);
(2)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟空气中的__________和___________发生反应。
(3)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法。这些方法都能防止锈蚀的共同原理是________________________;
(4)炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如下:
请写出第③步反应的化学方程式:____________________________________;
(5)金属矿物的储量有限,而且不能再生;目前世界上已有50%以上的废钢铁得到回收利用,其目的是_____________________________(填“合理开采矿物”或“节约金属资源”)。