下列化学用语或模型正确的是
A.氯化氢的电子式: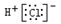 |
B.N2的结构式:N≡N |
C.硫离子结构示意图: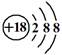 |
D.CH4分子的球棍模型: |
门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是
| A.X单质不易与水反应 | B.XO2可被碳或氢还原为X |
| C.XCl4的沸点比SiCl4的高 | D.XH4的稳定性比SiH4的高 |
常温下,将CO2通人2LpH=12的KOH溶液中。溶液中水电离出的OH-离子浓度(φ)与通入的CO2的体积(V)的关系如下图所示。下列叙述不正确的是
| A.a点溶液中:水电离出的c(H+)=1×10-12mol/L |
| B.b点溶液中:c(H+)=1×10-7mol/L |
| C.c点溶液中:c(K+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] |
| D.d点溶液中:c(K+)=2c(CO32-)+c(HCO3-) |
下列有关物质性质、结构的表述均正确,且存在因果关系的是
| 表述I |
表述Ⅱ |
|
| A |
同一主族元素原子的最外层电子数相同 |
在形成化合物时,同一主族元素的化合价都相同 |
| B |
在水中,KCl的溶解度比I2的溶解度大 |
KCl晶体中Cl-与Na+间的作用力大于碘晶体中分子间的作用力 |
| C |
P4O10、C6H12O6(葡萄糖)均属于非电解质 |
P4O10、C6H12O6的水溶液均不导电 |
| D |
Si的原子半径比C的大,Si与H之间的键能比C与H间的小 |
通常条件下,CH4分子比SiH4分子稳定性高 |
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
下列说法不正确的是
| A.放电时,电极A为负极 |
| B.根据上表数据,该电池工作的适宜温度应控制在350~2050℃ |
| C.充电时,Na+的移动方向为从电极B到电极A |
| D.充电时,总反应为Na2Sx==2Na+xS(3<x<5),则阳极的电极反应式为Sx-2e-==xS |
将一定量的NO2充入注射器中后封口,下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。已知反应:2NO2(红棕色) N2O4(无色) △H<0。下列说法正确的是
N2O4(无色) △H<0。下列说法正确的是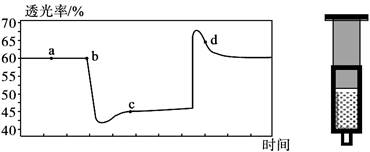
| A.b点的操作是拉伸注射器 |
| B.c点与a点相比,c(NO2)增大,c(N2O4)减小 |
| C.d点:υ(正)> υ(逆) |
| D.若注射器绝热(不与外界进行热交换),则压缩达新平衡后平衡常数K值减小 |