X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g • L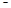 1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是
1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2 。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
对于某些离子的检验及结论正确的是
| A.加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中一定有CO32— |
| B.加氯化钡溶液有白色沉淀产生,再加盐酸,淀淀不消失,原溶液中一定有SO42- |
| C.加盐酸无现象,再加氯化钡溶液有白色沉淀产生,原溶液中一定有SO42- |
| D.加入AgNO3溶液后有白色沉淀,原溶液中一定有Cl— |
下列针对H3O+的说法中正确的是
| A.中心原子上的孤电子对数为2 |
| B.O原子采用sp2杂化, 空间构型为三角锥形 |
| C.离子中存在配位键 |
| D.纯水呈中性, 纯水中不存在H3O+微粒 |
设NA为阿伏加德罗常数,下列说法不正确的是
| A.18gH2O中含有的电子数为10 NA |
| B.46gNO2和46gN2O4含有的原子数均为3 NA |
| C.1L 1mol·L-1的盐酸中,所含HCl分子数为NA |
| D.标准状况下,11.2L O3中含1.5 NA个氧原子 |
下列化合物中既含有离子键又含有极性共价键和配位键的是
| A.NaCl | B.H2SO4 | C.Na2O2 | D.NH4Cl |
下列物质的分子中既有σ键,又有π键的是
①HCl②H2O③N2④H2O2⑤C2H4⑥C2H2
| A.①②③ | B.③④⑤⑥ | C.③⑤⑥ | D.①③⑥ |