标况下,在三个干燥的烧瓶内分别装入干燥纯净的NH3、含一半空气的氯化氢气体、NO2和O2的混合气体[V(NO2)∶V(O2)=4∶1]。倒扣在水槽中充分作用后,三个烧瓶中所得溶液的物质的量浓度之比为( )
| A.2∶1∶2 | B.5∶5∶4 | C.1∶1∶1 | D.无法确定 |
对可逆反应2A(s)+3B(g) C(g)+2D(g) △H<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) △H<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高.
| A.①② | B.④ | C.③ | D.④⑤ |
在下列各说法中,正确的是
A.对于2SO2(g)+O2(g) 2SO3(g)△H= —QkJ•mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2kJ 2SO3(g)△H= —QkJ•mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2kJ |
| B.热化学方程式中的化学计量数不能用分数表示 |
| C.Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,该反应的化学能可以转化为电能 |
| D.△H的大小与热化学方程式的化学计量数无关 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
| A.氢氧燃料电池在碱性介质中的负极反应式:H2-2e-=2H+ |
B.用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O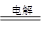 H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| D.钢铁发生吸氧腐蚀的负极反应式:Fe-2e-═Fe2+ |
有关热化学方程式书写与对应关系表述均正确的是
| A.稀醋酸与0.1mol•L-1NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H="+57.3" kJ•mol-1 |
| B.在101KPa下氢气的燃烧热△H="-285.5" kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H="+285.5" kJ•mol-1 |
| C.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)=FeS(s)△H="-95.6" kJ•mol-1 |
| D.已知2C(s)+O2(g)=2CO(g)△H="-221" kJ•mol-1,则可知C的燃烧热为110.5 kJ•mol-1 |
某原电池总反应的离子方程式为2Fe3++Fe=3Fe2+,能实现该反应的原电池是
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B.正极为C,负极为Fe,电解质溶液为FeSO4溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Cu,电解质溶液为CuSO4溶液 |