化合物HIn在水溶液中因存在电离平衡 HIn(溶液)(红色) H+(溶液)+In-(溶液)(黄色),故可用作酸碱指示剂。
H+(溶液)+In-(溶液)(黄色),故可用作酸碱指示剂。
浓度为0.02 mol·L-1的下列各溶液①盐酸②石灰水③NaCl溶液
④NaHSO4溶液⑤NaHCO3溶液⑥氨水,其中能使指示剂显红色的是:
| A.①④⑤ | B.②⑤⑥ | C.①④ | D.②③⑥ |
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如下图。下列叙述正确的是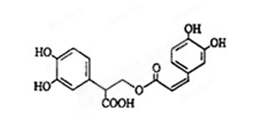
| A.迷迭香酸属于芳香烃 |
| B.1mol迷迭香酸最多能和9mol氢气发生加成反应 |
| C.迷迭香酸可以发生水解反应、取代反应和酯化反应 |
| D.lmol迷迭香酸最多能和含5mol NaOH的水溶液完全反应 |
某强氧化剂XO(OH)2+,被亚硫酸钠还原到较低价态。如果还原2.4×10-3 mol XO(OH)2+,需用30ml0.2 mol/L的亚硫酸钠溶液,还原后X的最终化合价为
| A.0 | B.+2 | C.-2 | D.+1 |
下列物质转化在给定条件下能实现的是
①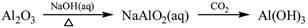
②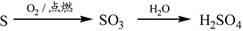
③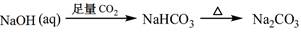
④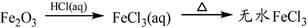
⑤
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
下列离子方程式书写正确的是
| A.Na2O2投入水中:2Na2O2+2H2O = 4Na++4OH−+ H2↑ |
| B.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O = HClO+HSO3- |
| C.钠投入CuSO4溶液中:2Na+Cu2++2H2O = 2Na++Cu(OH)2↓+H2↑ |
| D.铜和稀HNO3反应:3Cu+8H++2NO3-= 3Cu2++2NO2↑+4H2O |
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:
2NaClO3 + 4HCl = 2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是
| A.浓盐酸在反应中仅体现还原性 |
| B.氧化性:NaClO3 <ClO2 |
| C.每生成0.lmol ClO2转移0.5mol电子 |
| D.被氧化和被还原的物质的物质的量之比为1:1 |