物质的量浓度相同的下列溶液中,NH4+浓度最大的是( )
| A.NH4Cl | B.NH4HSO4 | C.CH3COONH4 | D.NH4HCO3 |
下列反应中,调节反应物用量或浓度不会改变反应产物的是
| A.H2S在氧气中燃烧 | B.铁在硫蒸气中燃烧 |
| C.二氧化硫通入石灰水中 | D.硫酸中加入锌粉 |
医疗上使用放射性核素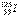 治疗肿瘤,该核素原子核内的中子数与电子数之差是
治疗肿瘤,该核素原子核内的中子数与电子数之差是
| A.19 | B.53 | C.72 | D.125 |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是()
A.NH4Cl的电子式: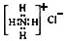 |
B.质量数为37的氯原子: |
| C.CO2的结构式:O=C=O | D.钾的原子结构示意图 |
在通常情况下能大量共存,并且可以用浓硫酸干燥的一组气体是()
| A.SO2、H2S、Cl2 | B.NO、O2、Cl2 |
| C.SO2、H2、N2 | D.HCl、CO、NH3 |
物质的下列变化,化学键不被破坏的是
| A.干冰气化 | B.HCl溶解于水 |
| C.食盐融化 | D.NH4Cl受热变成气体 |