下列各物质的名称正确的是 ( )
| A.3,3-二甲基丁烷 | B.2,3,3-三甲基丁烷 |
| C.2,2-二甲基-3-乙基丁烷 | D.2,3-二甲基-4-乙基己烷 |
下列说法正确的是()
| A.两种元素形成的离子晶体中不可能存在共价键 |
| B.氢键影响物质的物理性质,也决定其稳定性 |
| C.石墨比金刚石稳定的原因是石墨晶体中存在分子间作用力 |
| D.NaCl晶体中,每个Cl-周围同时吸引6个Na+ |
若NA表示阿佛加德罗常数,下列说法正确的是
| A.1 mol Cl2作为氧化剂得到的电子数为NA |
| B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子 |
| C.14 g氮气中含有7NA个电子 |
| D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
下列关于胶体的叙述不正确的是
| A.红色激光束能透过小烧杯中的氢氧化铁胶体,但不能透过小烧杯中较浓的硫酸铜溶液 | B.胶体的丁达尔效应是胶体粒子对可见光散射而形成的 |
| C.胶体化学是随20世纪未纳米科技兴起而产生的 | |
| D.纳米粒子的大小与胶体粒子相当,但纳米粒子的体系不一定是胶体 |
能正确表示下列反应的离子方程式是
A.将铜屑加入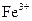 溶液中: 溶液中: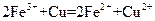 |
B.将磁性氧化铁溶于盐酸: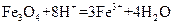 |
C.将氯化亚铁溶液和稀硝酸混合: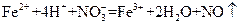 |
D.将铁粉加入稀硫酸中: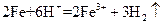 |
下列说法正确的是
| A.NaOH的摩尔质量是0.040Kg/mol |
| B.1mol H2的质量与它的相对分子质量相等 |
| C.1mol H2O的质量为18g /mol |
| D.氧气的摩尔质量在数值上等于它的相对分子质量 |