在FeCl3和CuCl2混合液中,加入过量的铁粉,充分反应后,溶液中的金属离子是( )
A Fe2+ B Fe3+ 和Fe2+ C Cu2+ 和Fe2+ D Cu2+
有BaCl2和KCl的混合溶液VL,将它分成两等份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗mmol H2SO4、nmol AgNO3。据此得知原混合溶液中的K+的物质的量浓度为 ( )
A.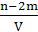 mol·L-1 mol·L-1 |
B.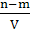 mol·L-1 mol·L-1 |
C.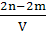 mol·L-1 mol·L-1 |
D.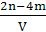 mol·L-1 mol·L-1 |
有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4 mol·L-1,S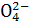 的物质的量浓度为0.7 mol·L-1,则此溶液中K+的物质的量浓度(mol·L-1)约为 ( )
的物质的量浓度为0.7 mol·L-1,则此溶液中K+的物质的量浓度(mol·L-1)约为 ( )
| A.0.1 | B.0.15 | C.0.2 | D.0.25 |
用98%的浓硫酸(密度为1.84 g·cm-3)配制1 mol·L-1的稀硫酸100 mL,配制溶液时可能用到的仪器有①玻璃棒;②胶头滴管;③100 mL容量瓶;④托盘天平;⑤50 mL烧杯;⑥10 mL量筒。则正确的选用顺序是 ( )
| A.⑥③⑤①② | B.⑥⑤③①② |
| C.④⑤③②① | D.⑥⑤①③② |
实验室需配制450 mL 0.1 mol·L-1的Na2CO3溶液,以下操作正确的是 ( )
| A.称取4.77 g Na2CO3固体溶于水配成450 mL溶液 |
| B.称取5.3 g Na2CO3固体溶于水配成500 mL溶液 |
| C.称取12.9 g Na2CO3·10H2O固体溶于水配成450 mL溶液 |
| D.量取90 mL 0.5 mol·L-1Na2CO3溶液加360 mL水稀释 |
下列说法中错误的是 ( )
| A.从1 L 1 mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol·L-1 |
| B.配制0.5 L 10 mol·L-1的盐酸,需要氯化氢气体112 L |
| C.0.5 L 2 mol·L-1BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D.10 g 98%的硫酸(密度为1.84 g·cm-3)与10 mL 18.4 mol·L-1硫酸的浓度是不同的 |