NA表示阿伏加德罗常数,以下说法中不正确的是
| A.25℃、1.01×105Pa时,NA个氢分子的体积约是22.4L |
| B.27g金属Al与足量的稀硫酸反应时生成的H2的分子数为1.5NA |
| C.常温常压下,n mol HD含有核外电子数为2NA |
| D.常温常压下,36g18O2中所含的中子数为20NA |
已知卤代烃可与金属钠反应,生成碳链较长的烃:R—X+2Na+R′—X → R—R′+2NaX
现有碘乙烷和1—碘丙烷混合物,使其与金属钠反应,生成的烃不可能是
| A.戊烷 | B.丁烷 | C.己烷 | D.2-甲基己烷 |
工业上以铝土矿(主要成分是Al2O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下: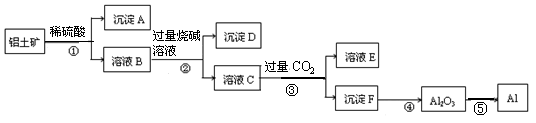
下列叙述错误的是
| A.沉淀A主要是SiO2 | B.步骤②的目的是分离Fe3+和Al3+ |
| C.溶液E溶质主要有碳酸钠和硫酸钠 | D.⑤主要是把电能转化为化学能 |
下列说法正确的是
①植物油和裂化汽油都可以使溴水褪色;②葡萄糖、油脂和蛋白质都能发生水解反应;③按汽油、煤油、柴油的顺序,含碳量逐渐增加;④防腐剂福尔马林(含甲醛)可用作食品保鲜剂;⑤乙醇、乙酸、乙酸乙酯都能发生取代反应
| A.①③⑤ | B.①②⑤ | C.②④⑤ | D.②③④ |
取一小段镁带,用砂纸除去表面的氧化膜,放入试管中。向试管中加入2mL水,并滴入2滴酚酞试液。一会儿后发现镁带表面有气泡放出,且镁带附近溶液变红色。加热试管至水沸腾。发现镁带表面有大量气泡放出,且试管中的液体全部变为浅红色。关于该实验下列说法不正确的是
| A.温度越高,镁与水反应的速率越快 |
| B.镁与水反应的化学方程式为:Mg+2H2O ="==" Mg(OH)2+H2↑ |
| C.氢氧化镁显碱性,且在水中有一定的溶解性 |
D.氢氧化镁是离子化合物,它的电子式可表示为: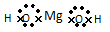 |
海水开发利用的部分过程如图所示。下列说法错误的是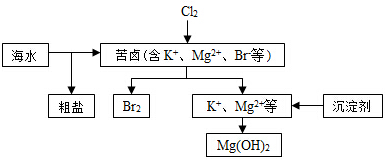
| A.向苦卤中通入Cl2是为了提取溴 |
| B.工业生产中常选用NaOH作为沉淀剂 |
| C.粗盐可采用除杂和重结晶等过程提纯 |
D.富集溴一般先用空气和水蒸气吹出单质溴,再用 将其还原吸收 将其还原吸收 |