下列说法中正确的是(NA为阿伏加德罗常数)
| A.78 gNa2O2晶体中所含阴阳离子个数均为2NA |
| B.1.5 g CH3+中含有的电子数为NA |
| C.3.4 g氨中含有0.6NA个N—H键 |
| D.常温下,100 mL1 mol·L-1AlCl3溶液中阳离子总数小于0.1NA |
甲醇、空气和强碱溶液做电解质的手机燃料电池中所发生的反应为:
2CH3OH+3O2+4OH-  2CO32-+6H2O,下列有关说法正确的是
2CO32-+6H2O,下列有关说法正确的是
| A.放电时,CH3OH参与反应的电极为正极 |
| B.放电时,负极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
| C.充电时,电解质溶液的pH逐渐增大 |
| D.放电时,每通入标况下11.2L O2完全反应转移电子数为1mol |
近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为:KI + 3H2O  KIO3 + 3H2↑。下列有关说法正确的是
KIO3 + 3H2↑。下列有关说法正确的是
| A.电解时,石墨作阴极,不锈钢作阳极 |
| B.电解时,阳极反应是: I – – 6e – + 3H2O = IO3 – + 6H+ |
| C.溶液调节至强酸性,对生产有利 |
| D.电解前后溶液的pH几乎不变 |
短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
| A.元素W、X的氯化物中,各原子均满足8电子的稳定结构 |
| B.元素X的一种单质是自然界中硬度最大的物质 |
| C.元素Y的单质只能与盐酸等酸反应生成氢气,而不能和碱反应 |
| D.元素Z可与元素X形成共价化合物XZ2 |
下列实验现象预测正确的是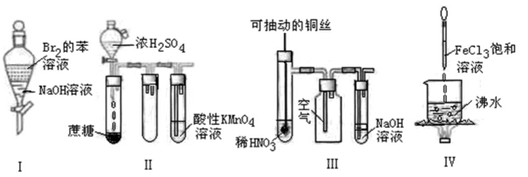
| A.实验I:振荡后静置,上层溶液颜色保持不变 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g),在温度673 K、压强30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是
2NH3(g),在温度673 K、压强30 MPa下,n(NH3)和n(H2)随时间t变化的关系示意图如图所示。下列叙述中正确的是
| A.c点处正反应速率和逆反应速率相等 |
| B.a点处正反应速率比b点处的大 |
| C.d点(t1时刻)和e点(t2时刻)处n(N2)不同 |
| D.t2点时刻,正反应速率大于逆反应速率 |