2.22克某元素的氯化物XCl2溶于水形成溶液后,加入40ml 1mol/L AgNO3溶液恰好完全反应。已知该元素原子核内的质子数和中子数相等。
(1)求X元素的质子数和质量数
(2)写出X元素在周期表中的位置
(6分)在隔绝空气的条件下,某同学将一块被氧化钠覆盖的钠块用一张无保护膜并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待反应完全后,在容器中收集到1.12L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27g,水槽和容器内溶液的总体积为2.0L,溶液中NaOH的浓度为0.050mol·L-1(忽略溶解的氢气的量)。试通过计算确定该钠块中钠元素的质量分数。
(4分)将一定质量铜与100 mL一定浓度的硝酸反应,铜完全溶解时产生的NO和NO2混合气体在标准状况下的体积为11.2 L。待产生的气体全部释放后,向溶液加入140mL 5 mol·L-1的NaOH溶液,恰好使溶液中的Cu2+ 全部转化成沉淀,求原硝酸溶液的物质的量浓度是多少。
(8分) Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。
⑴正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含mg FeSO4·7H2O的片剂。
⑵“速力菲”是市场上一种常见的补铁药物,其中Fe2+的含量为35.0%。该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率超过10%即不能再服用。为检验某药店出售的“速力菲”是否失效,取10.00g该药品全部溶于稀硫酸,配制成1000mL溶液。取其中20.00mL,用0.01000 mol/L KMnO4溶液滴定,用去KMnO4溶液24.00mL。通过计算说明该药物是否能服用?(MnO4-在酸性条件下的还原产物为Mn2+,药品中除Fe元素外其他成分不与KMnO4反应)
在室温下,向200mL Cu(IO3)2饱和溶液中加入一定浓度100 mL(经酸化)的KI溶液,发生如下反应:
5I-+IO3-+6H+=3I2+3H2O
2Cu2++4I-=2CuI↓+I2
充分反应后,再加入25.0mL 0.234 mol/L KIO3溶液恰好将过量的KI反应掉。再从上述所得混合液中取出25.0 mL,用0.110 mol/L Na2S2O3溶液滴定,发生反应
I2+2S2O32-=2I-+S4O62-
消耗了30.0mL Na2S2O3溶液。溶液体积改变忽略不计。计算:
(1)原饱和溶液中Cu(IO3)2的物质的量浓度;
(2)若Cu(IO3)2饱和溶液的的密度为1.00g/cm3,Cu(IO3)2的溶解度是多少?
接触法制硫酸,最后的产品是质量分数为98%的硫酸或20%的发烟硫酸(H2SO4和SO3的混合物,其中含20%的SO3)。若98%的硫到可表示为SO3·aH2O,20%的发烟硫酸可表示为SO3·bH2O,
则a,b的值(a、b可用分数表示)分别是:a=_________,b=____________;用
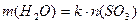 分别表示SO3转化成上述两种硫酸时,用水的质量与SO3物质的量的关系式分别是:
分别表示SO3转化成上述两种硫酸时,用水的质量与SO3物质的量的关系式分别是: =______
=______ ,
,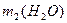 =______
=______ ;
;若工厂同时生产上述两种硫酸,则两种产品的质量比x(
 ,
,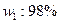 的硫酸的质量,
的硫酸的质量, 的发烟硫酸的质量)与
的发烟硫酸的质量)与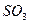 用量之比的关系是:
用量之比的关系是: ___________x;
___________x;实际生产时,总
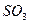 的物质的量一定,x随市场需求而有改变,则用水总量
的物质的量一定,x随市场需求而有改变,则用水总量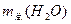 、x、
、x、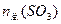 的关系式是_________________。
的关系式是_________________。