下列实验设计及其对应的离子方程式均正确的是()
| A.用FeCl3溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| C.NH4HSO3溶液与足量NaOH溶液混合加热: NH4++HSO3-+2OH-  NH3↑+SO32-+2H2O NH3↑+SO32-+2H2O |
| D.将氯气溶于水制备次氯酸:Cl2+H2O=2H++Cl-+ClO- |
有一混合物的水溶液,只可能含以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42 -,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。
根据上述实验回答: ___________, 不能确定是否存在的离子是________________。
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):
离子符号______,浓度_____________;
离子符号______,浓度_______________;
离子符号______,浓度________________;
(3)试确定K+ 是否存在________(填“是”或“否”),判断的理由是 ______________。
镁铁混合物13.8g溶解在足量某浓度的稀硝酸中,完全反应,其还原产物只有一氧化氮(0.3mol),则向反应后的溶液中加入足量的NaOH溶液,可生成的沉淀质量为
| A.26 | B.29.1g | C.29.5g | D.24g |
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固。化学家由此得到启发,从腐败草料中提取出结构简式为右下图所示的双香豆素。下列关于双香豆素的推论中错误的是
| A.有望将它发展制得一种抗凝血药 |
| B.它无嗅并略具芳香味,因而可用来制备致命性出血型的杀鼠药 |
C.它可由化合物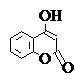 和甲醛(HCHO)通过缩合反应制得 和甲醛(HCHO)通过缩合反应制得 |
| D.它与足量NaOH溶液反应,消耗NaOH 6mol |
百服宁口服液为解热镇痛药,主要用于治疗头痛、发烧。其主要化学成分的结构简式如下,下列有关该有机物的叙述正确的是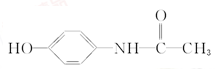
| A.分子式为C8H10NO2 |
| B.该有机物属于α-氨基酸 |
| C.该有机物属于α-氨基酸的同分异构体有3种 |
| D.该有机物与FeCl3溶液发生显色反应 |
在给定的溶液中,离子能大量共存的是
| A.滴加甲基橙显红色的溶液:I-、NH4+、Cl-、NO3- |
| B.含有大量AlO2-的溶液:Na+、K+、NO3-、CO32- |
| C.常温下由水电离出来的c(H+)=10-13 mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.含有溶质为NaHSO4的溶液:K+、SiO32-、NO3-、Al3+ |