下列关于碱金属的电子结构和性质的叙述中不正确的是( )
| A.碱金属原子最外层都只有一个电子,在化学反应中容易失去 |
| B.都是强还原剂 |
| C.都能在O2中燃烧生成过氧化物 |
| D.都能与水反应生成碱 |
下列各式中属于正确的水解反应离子方程式的是
A.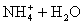 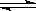 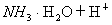 |
B.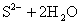 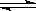 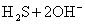 |
C. 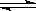 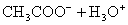 |
D. 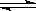 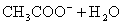 |
.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 + Pb + 2H2SO4 = 2PbSO4↓+ 2H2O,根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb + SO42- - 2e - = PbSO4↓ |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
25℃时,将稀氨水逐滴加入稀盐酸中,当溶液的pH=7时,下列关系不正确的是
| A.c(NH4+)=c(Cl-) | B.c(H+)=c(OH-) |
| C.c(NH4+)<c(Cl-) | D.c(OH-)+c(Cl-)=c(H+)+(NH4+) |
在蒸发皿中加热蒸干并灼烧(低于400℃)下列物质的溶液,可以得到该物质固体的是
| A.氯化铝 | B.碳酸钠 | C.碳酸氢钠 | D.高锰酸钾 |
已知Zn(OH)2的溶度积常数为1.2×10-17(mol·L-1)3,则Zn(OH)2在水中的溶解度为
A .1.4×10-6mol·L-1B.2.3×10-6mol·L-1
.1.4×10-6mol·L-1B.2.3×10-6mol·L-1
C.1.4×10-9mol·L-1 D.2.3×10-9mol·L-1