A、B、C、D、E五种元素在周期表里的位置如下表所示:A、B、C为同主族元素,A为该族中原子半径最小的元素;D、B、E为同周期元素,E为该周期中原子半径最小的元素。D元素名称是 ,在周期表第 周期,第 族,其原子结构示意图 。
| |
A |
|
| D |
B |
E |
| |
C |
|
金属钛(Ti)因为具有许多神奇的性能越来越引起人们的关注,被誉为“未来金属”。常温下钛不和非金属、强酸反应,加热至红热时,能与常见的非金属反应。工业上由钒钛磁铁矿经“选矿”得到的钛铁矿(主要成分为FeTiO3)制取金属钛的主要工艺过程如下: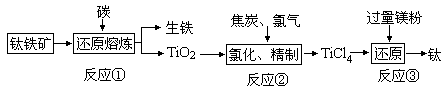
(1)从金属矿石中提炼金属一般需要经过三个阶段,上述工艺溶度积中涉及的有矿石中金属元素的还原、矿石的富集、金属的精炼;没有涉及的一个阶段是______________;生铁实际上属于铁______等元素形成的合金。若生产中碳的氧化产物主要为一种可燃性气体,请写出反应②的化学方程式__________________________。
(2)生产中碳除了用还原剂还原还原金属矿物外,还有一个重要作用是______________;反应③是在氩气的环境中进行,目的是_____________________,如何从反应③后的固体中获得金属钛_______________________________。
(3)已知在氯化过程中还有一种副产物VOCl3生成,实际生产中常在409K时用铜还原VOCl3,得到不溶于TiCl4的VOCl2,当有1molCu参加反应时转移的电子数为NA,试写出该反应的化学方程式为___________________。
使用化石燃料的汽车在给人类带来便利的同时,其排放出的尾气也会污染环境,降低汽车尾气有害成份是减轻大气污染的重要途径;研制开发使用新型能源的汽车更具有现实意义。
(1)已知下列热化学方程式:
2CO(g)+O2(g)=2CO2(g)ΔH=-566 kJ·mol-1
N2 (g)+O2(g)=2NO(g)ΔH=+27kJ·mol-1
加装有催化转化器的汽车尾气排放时反应方程式为:2NO(g)+2CO(g) N2(g)+2CO2(g) ,该反应的ΔH为________;假设此变化过程热量变化共有59.3kJ,则转移的电子为______NA(NA表示阿伏加德罗常数)。
N2(g)+2CO2(g) ,该反应的ΔH为________;假设此变化过程热量变化共有59.3kJ,则转移的电子为______NA(NA表示阿伏加德罗常数)。
(2)某科研机构在实验室中对NO、CO之间的反应进行了探究:他们将2molNO、1molCO充入一个1L固定容积的容器中,测出反应过程中各物质的浓度变化并绘制成右图(0~15min内)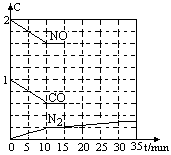
①此温度下该反应的平衡常数为__________;15min时,改变某种条件后c(N2)变化如右图(15min~35min)所示,则改变的条件可能是____
a.降低温度 b.缩小容器容积
c.增加CO2的量 d.升高温度
②若N2在0~5分钟、10~15分钟、15~30、30~35分钟的平均反应速率分别记为 (0~5)、
(0~5)、 (10~15)、
(10~15)、 (15~30)、
(15~30)、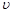 (30~35)。四者之间的大小关系为________________,
(30~35)。四者之间的大小关系为________________,
③若保持温度不变,在12min时再向容器中充入CO、N2各0.6mol,则平衡将___________移动(填“向左”、“向右”、“不”)。
(3)高铁电池具有能量密度高、原料丰富成本低廉,绿色无污染不需要回收等特点,它己成为电动汽车首选的电池,其工作原理为:3Zn+2K2FeO4+8H2O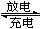 3Zn(OH)2+4KOH
3Zn(OH)2+4KOH
+2Fe(OH)3。则放电时,负极材料是________,正极上的电极反应式为_________________充电时阴极附近溶液pH_______(填增大、减小、不变)。
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
CO(g) + 2H2(g)  CH3OH(g)
CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同)__________。
| A.生成CH3OH的速率与消耗CO的速率相等 |
| B.混合气体的密度不变 |
| C.混合气体的相对平均分子质量不变 |
| D.CH3OH、CO、H2的浓度都不再发生变化 |
E. 容器中气体的压强不再改变
(2)下表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
①由表中数据判断该反应的△H__________0(填“>”、“="”" 或“<”);
②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO) =" 0.2" mol/L,则CO的转化率为__________,此时的温度为__________。
(3)要提高CO的转化率,可以采取的措施是__________。
a. 升温 b. 加入催化剂
c. 增加CO的浓度 d. 恒容下加入H2使容器内压强变大
e. 分离出甲醇 f. 恒容下加入惰性气体使容器内压强变大
(4)在250℃时,某时刻测得该温度下的密闭容器中各物质的物质的量浓度见下表:
| CO |
H2 |
CH3OH |
| 0.5 mol·L-1 |
2mol·L-1 |
6mol·L-1 |
此时反应的正、逆反应速率的关系是:v(正)v(逆)(填“>”、“="”" 或“<”)。
(5)如图1所示,甲为恒容密闭容器,乙为恒压密闭容器。在甲、乙两容器中分别充入等物质的量的H2和CO,使甲、乙两容器初始容积相等。在相同温度下发生上述反应,并维持反应过程中温度不变。在图2中标出甲、乙两容器中CO的转化率随时间变化的对应图像(在图2相应曲线右侧的框格中分别标注“甲”、“乙”)。
超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO = 2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| c(NO)/(mol/L) |
1.00×10-3 |
4.50×10-4 |
2.50×10-4 |
1.50×10-4 |
1.00×10-4 |
1.00×10-4 |
| c(CO)/(mol/L) |
3.60×10-3 |
3.05×10-3 |
2.85×10-3 |
2.75×10-3 |
2.70×10-3 |
2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的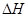 ______0(填写“>”、“<” 或“=”)。
______0(填写“>”、“<” 或“=”)。
(2)前2s内的平均反应速率v(N2)=_____________。
(3)该反应的平衡常数K的表达式为K=_________________________;在该温度下,反应的平衡常数的值为____________
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是______
A. 选用更有效的催化剂 B. 升高反应体系的温度
C. 降低反应体系的温度 D. 缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面的实验设计表中。请在表格中填入剩余的实验条件数据。
| 实验编号 |
T/℃ |
NO初始浓度 mol·L-1 |
CO初始浓度 mol·L-1 |
催化剂的比表面积 m2·g-1 |
| Ⅰ |
280 |
1.20×10-3 |
5.80×10-3 |
82 |
| Ⅱ |
124 |
|||
| Ⅲ |
350 |
124 |
把煤作为燃料可通过下列两种途径:
途径I:直接燃烧:C(s)+O2(g) = CO2(g)
途径II:先制水煤气:C(s) + H2O(g) =" CO(g)" + H2(g)
燃烧水煤气:2 CO(g) + O2(g)=2CO2(g); 2H2(g)+O2(g) = 2H2O(g)
已知:①C(s)+O2(g) = CO2(g);△H1=-393.5kJ·mol-1
②H2(g) + 1/2 O2(g) = H2O(g);△H2=-241.8kJ·mol-1
③CO(g) + 1/2 O2 (g)= CO2(g);△H3=-283.0kJ·mol-1
请回答下列问题:
(1)C(煤)的标准燃烧热是
(2)根据盖斯定律写出煤和气态水生成水煤气的热化学方程式:
(3)在制水煤气反应里,反应物具有的总能量________(填“>”、“<”或“=”)生成物所具有的总能量。
(4)根据两种途径,下列说法错误的是 (单选)
| A.途径II制水煤气时增加能耗,故途径II的做法不可取 |
| B.与途径I相比,途径II可以减少对环境的污染 |
| C.与途径I相比,途径II可以提高煤的燃烧效率 |
| D.将煤转化为水煤气后,便于通过管道进行运输 |