下列说法中正确的是 ( )
| A.用铁与稀硝酸反应来制备氢气 |
| B.SO2能使湿润的蓝色石蕊试纸先变红后退色 |
| C.NO2 溶于水发生了氧化还原反应,它既是氧化剂又是还原剂 |
| D.钠在氧气中燃烧发出白光,生成白色固体氧化钠 |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),60s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),60s达到平衡,生成0.3 mol Z,下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001 mol/(L·s) |
B.将容器体积变为20 L,Z的平衡浓度变为原来的 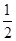 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的ΔH>0 |
对于任何一个平衡体系,采用以下措施,一定会使平衡移动的是
| A.升高温度 | B.加入一种反应物 |
| C.对平衡体系增加压强 | D.使用催化剂 |
反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率增大的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率增大的是
| A.增加C的量 | B.将容器的体积缩小一半 |
| C.保持体积不变,充入N2 | D.保持压强不变,充入N2 |
在2A+B 3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol/(L·s) B.v(B)= 0.3 mol/(L·s)
C.v(C)=0.8 mol/(L·s) D.v(D)=1 mol/(L·s)
室温下将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)= CuSO4(s)+5H2O(l), 热效应为△H3。则下列判断正确的是
| A.△H2>△H3 | B.△H1>△H3 |
| C.△H1 =△H2+△H3 | D.△H1+△H2>△H3 |