T℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是
A.T℃时,该反应的化学方程式为:X(g)+Y(g) 2Z(g),平衡常数K=4 2Z(g),平衡常数K=4 |
| B.平衡时X、Y的转化率相同 |
| C.达到平衡后,恒温将容器体积扩大为3 L,平衡向逆反应方向移动 |
| D.T ℃时,若起始时X为0.60mol,Y为1.00 mol,则平衡时Y的 |
转化率小于80%
下列各种冶炼方法中,可制得相应金属的为()
| A.加热氢氧化铝 | B.加热碳酸钙 |
| C.电解饱和食盐水 | D.电解熔融氯化镁 |
为亚硝酸盐会使Fe2+离子转变成Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有()
| A.酸性 | B.碱性 | C.氧化性 | D.还原性 |
工业上用铝土矿(主要成分为Al2O3·xH2O,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,提取时操作过程如下图,指出图中操作错误的是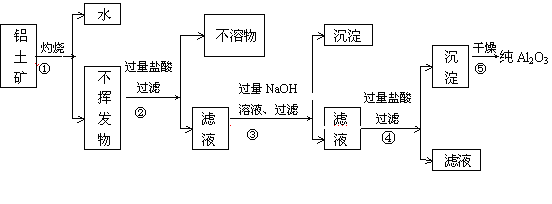
| A.④⑤ | B.③④ | C.②⑤ | D.①② |
由锌、铁、铝、镁四种金属中的两种组成的混和物10克,与足量的盐酸反应产生的氢气在标准状况下为11.2升,则混和物中一定含有的金属是
| A.锌 | B.铝 | C.铁 | D.镁 |
下列物质均有漂白作用,其漂白原理相同的是 ( )
①过氧化钠②次氯酸③二氧化硫④活性炭⑤臭氧
| A.①②⑤ | B.①③⑤ | C.②③④ | D.①②③ |