如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题:
(1)打开K2,闭合K1,B为__________极,A的电极反应为______________,最终可观察到的现象是 。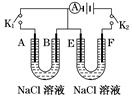
(2)打开K1,闭合K2,E为________极,检验F极产生气体的方法是 。
(3)若往U型管中滴加酚酞,进行(1)、(2)操作时, 极周围能变红(填A、B、E、或F,下同)。若滴加K3[Fe(CN)6]溶液,在 极周围溶液变为 色。
(4)若电源选用燃料电池,结构如图,以熔融碳酸盐为电解质(能够传导CO32-),电池工作时电解质组成保持稳定,请写出正极反应的方程式 ,若在标况下消耗11.2L的甲烷,电解NaCl溶液产生的H2的物质的量为 mol(假设燃料电池能量转化率为75%)。
xk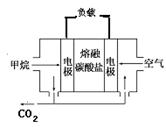
以下是一些烷烃的燃烧热(kJ/mol)数据,回答下列问题:
| 化合物 |
燃烧热 |
化合物 |
燃烧热 |
| 甲烷 |
891.0 |
正丁烷 |
2 878.0 |
| 乙烷 |
1 560.8 |
异丁烷 |
2 869.6 |
| 丙烷 |
2 221.5 |
2甲基丁烷 |
3 531.3 |
(1)物质的能量越高越不稳定,比较正丁烷、异丁烷的热稳定性:正丁烷________异丁烷(填“>”或“<”)。
(2)写出表示乙烷燃烧热的热化学方程式:_________________________________
(3)相同质量的烷烃,碳的质量分数越大,燃烧放出的热量________(填“越多”“越少”或“相同”)。
二氧化碳“组合转化”的某烷烃碳架结构如图所示: ,此烷烃的一溴代物有种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为,
,此烷烃的一溴代物有种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为,
在乙醇的化学性质中,各反应的断键方式可概括如下: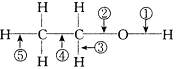
⑴消去反应:;⑵与金属反应:;
⑶催化氧化:;⑷分子间脱水:;
⑸与HX反应:。
莽草酸的结构式如图: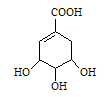 ,请回答:
,请回答:
(1)写出莽草酸分子中官能团名称。
(2)该有机物分子1moL最多能和moL NaOH发生反应。
以下是以莽草酸A为原料的有机合成路线: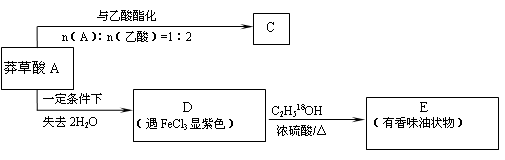
已知D的碳环上一氯代物只有两种。请继续回答下列问题:
(3)C有三种同分异构体,写出其中的一种结构简式。
(4)莽草酸A→D的反应类型是:。
(5)写出下列反应的化学方程式:
① D与足量的NaHCO3溶液反应;
② D→E。
根据下列的有机物合成路线回答问题: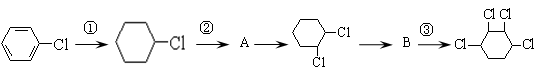
(1)写出A、B的结构简式:
A、B。
(2)写出各步反应类型:
①、②、③。
(3)写出②、③的反应方程式:
②,③。