元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
| A.左、下方区域的金属元素 | B.稀有气体元素 |
| C.右、上方区域的非金属元素 | D.金属元素和非金属元素分界线附近的元素 |
将下列液体分别与溴水充分混合并振荡,静置后上层液体呈现橙色,下层液体是无色的是
| A.CCl4 | B.苯 | C.戊烯 | D.乙醇 |
按系统命名法,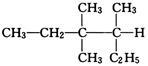 的正确名称是
的正确名称是
| A.3,3,4-三甲基己烷 | B.3,3-二甲基-2-乙基戊烷 |
| C.3,4,4-三甲基己烷 | D.3,3-二甲基-4-乙基戊烷 |
与CH3 CH2CH=CH2互为同分异构体的是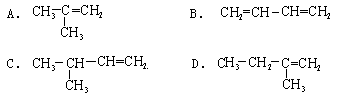
在光照条件下,将1mol甲烷和1mol氯气混合充分反应后,得到的产物为
| A.CH3Cl、HCl | B.HCl、CCl4 |
| C.CH3Cl、CH2Cl2 | D.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl |
下列有关化学用语表示正确的是
| A.乙烷的结构式:C2H6 |
| B.3—甲基—1—丁烯的结构简式:(CH3)2CHCH=CH2 |
C.乙炔的电子式: |
D.乙醇分子的比例模型: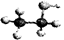 |