节约资源和保护环境已经成为我们的基本国策。节能减排、环境保护和生态市建设是市政府近些年的工作重点。硫酸厂生产硫酸的流程是:把含硫矿物燃烧,生成二氧化硫,二氧化硫和氧气在高温和催化剂的作用生成三氧化硫,最后三氧化硫和水化合生成硫酸。写出三氧化硫和水化合生成硫酸的化学方程式
某纯碱样品中含有少量硫酸钠,现欲测定其碳酸钠的质量分数,利用含有少量硫酸的澄清废水进行如下实验:
《实验原理》Na2CO3+H2SO4 = Na2SO4 + H2O + CO2↑通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数。
《实验装置》
《实验步骤》
①如图连接装置(除B、C外)并加入所需药品。
②称量并记录B的质量(m1)。(称量时注意封闭B的两端。)
③按动鼓气球,持续鼓入空气约1分钟。
④连接上B、C。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质量(m2)。(称量时注意封闭B的两端及E右端的出口。)
⑧计算。
⑴已知碱石灰的主要成分是氢氧化钙和氢氧化钠,则干燥管A的作用是: ,以免使测定结果偏大。
(2) (能或不能)用稀盐酸代替稀硫酸,因为盐酸具有 性,会使测得碳酸钠的质量分数 (填偏大、偏小或不变,下同);若去除干燥管C,则测得碳酸钠的质量分数将会
(3)E装置的作用是
(4)本实验能否省略③、⑥两个步骤? (填能或不能),原因分别是 、
(5)若所取样品的质量为6g,分液漏斗F中盛放5%只含硫酸一种溶质的澄清废水,称得m1为51.20g,m2为53.40g,(计算结果保留两位小数)
求:(1)样品中碳酸钠的质量分数为多少?
(2)D装置中正好反应后,所得溶液的溶质质量分数是多少?
水是生命之源,是自然界中重要的物质。
Ⅰ.温泉的利用是人们开发地热的一种形式,南京汤山温泉具有悠久的文化。
(1)清澈的温泉水是(填“纯净物”或“混合物”)。
(2)净化温泉水的过程中,会使用到活性炭,主要是利用其作用。
(3)鉴别温泉水是硬水还是软水需加入的试剂是。
Ⅱ.海水是巨大的资源宝库。海水晾晒可得到粗盐,已知某粗盐样品中除泥沙外还含有Na2SO4、MgCl2、CaCl2等杂质。实验室提纯流程如下: 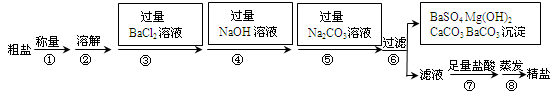
(1)用托盘天平称量10.2g粗盐样品时,若指针偏向左边,则表示(填字母序号)。
| A.右盘重,砝码轻 | B.右盘轻,样品少 |
| C.左盘重,样品多 | D.左盘轻,砝码重 |
(2)第④步操作发生反应的化学方程式是。
(3)第⑤步操作的目的是。
(4)在第⑦步操作中,向滤液中滴加足量盐酸的目的是。
Ⅲ.水也是一种重要的原料。某工厂用电解水的方法来制取氧气,若制取100kg氧气,理论上消耗水的质量是多少?(写出计算过程)
用100g含杂质3.2%的生铁粉(杂质不参与反应),与质量分数为10%的稀硫酸恰好完全反应制硫酸亚铁。求消耗的稀硫酸质量。
我市锰矿资源丰富,MnO2是一种无机功能材料,主要用于制造干电池。当地某工厂加工得到了粗MnO2(主要含有杂质MnCO3,其它杂质忽略不计),为了测定其中MnO2的含量,称取57.5g粗MnO2样品,加入足量的稀硫酸溶液,产生CO2气体4.4g。
(已知:MnCO3+ H2SO4  MnSO4+H2O+CO2↑)
MnSO4+H2O+CO2↑)
试完成下列问题:(1)计算57.5g粗MnO2中含有MnCO3的质量,
(2)计算粗MnO2中的MnO2的质量分数。
将117.0g氯化钠溶液与140.0g的硝酸银溶液混合,恰好完全反应,过滤后所得溶液的质量为228.3g。计算该氯化钠溶液的溶质质量分数?
(反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3)
某硫酸厂废水中含有少量硫酸.排放前,技术员小张先对废水中硫酸的含量进行检测。
(1)配制溶液:
欲配制溶质质量分数为4%的NaOH溶液100g,需要NaOH固体g,水ml
(水的密度为1 g/CI113);
(2)检测分析:
取废水样品98g,向其中逐滴加入NaOH溶液至恰好完全反应时,消耗4%的NaOH
溶液20g(假设废水中其它成分均不和NaOH反应)。试计算废水中硫酸的质量分数
(写出计算过程)。