如图I所示,甲、乙之间的隔板K和活塞F都可以左右移动,甲中充入2 molA和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。在一定条件下发生反应:2A(g)+B(g) 2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是
2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是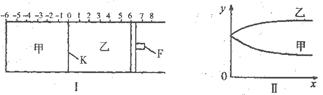
| A.达到平衡时,隔板K最终停留在刻度0与-2之间 |
| B.若达到平衡时,隔板K最终停留在刻度-l处,则乙中C的转化率小于50% |
| C.若达到平衡时,隔板K最终停留在靠近刻度-2处,则乙中F最终停留刻度大于4 |
| D.若图Ⅱ中x轴表示时间,则y轴可表示甲、乙两容器中气体的总物质的量或A的物质的量 |
下列各组物质中,都是共价化合物的是()
| A.H2S和Na2O2 | B.H2O2和CaF2 | C.NH3和N2 | D.HNO3和HClO3 |
AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子满足8电子结构,则下列说法正确的是()
| A.AB3是三氧化硫 |
| B.A是ⅢA族元素 |
| C.B原子比A原子多10个电子 |
| D.B的氢化物和A的氢化物都不易溶于水 |
下列说法正确的是()
| A.离子化合物中只能含离子键,不能有共价键 |
| B.所有非金属之间形成的化学键一定是共价键 |
| C.电子数相同的两种微粒一定是同一元素 |
| D.判断化学变化的可靠方法是看有无化学键的变化 |
X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是()
| A.元素非金属性由强到弱的顺序为. Z>Y>X |
| B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C.3种元素的气态氢化物中,Z的气态氢化物最稳定 |
| D.原子半径有大到小的顺序为Z.>Y>X |
把a,b,c,d四块金属片浸入稀硫酸中,用导线两两相连组成原电池.若a,b相连时,a为负极;c,d相连时,d上产生大量气泡;a.c相连时,电流由c经导线流向a;b、d相连时,电子由d经导线流向b,则此四种金属的活动性由强到弱的顺序为
| A.a>b>c>d | B.a>c>d>b |
| C.c>a>b>d | D.b>d>c>a |