下列判断错误的是
| A.沸点:NH3>PH3>AsH3 | B.熔点:Si3N4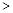 NaCl NaCl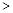 SiI4 SiI4 |
| C.酸性:HClO4>H2SO4>H3PO4 | D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
下列叙述正确的是
| A.离子晶体中,只存在离子键,不可能存在其它化学键 |
| B.在卤族元素(F、Cl、Br、I)的氢化物中,HF的沸点最低 |
| C.NaHSO4、Na2O2晶体中的阴、阳离子个数比均为1 : 2 |
| D.晶体熔点:金刚石>食盐>冰>干冰 |
在下列有关晶体的叙述中错误的是
| A.离子晶体中,一定存在离子键 | B.原子晶体中,只存在共价键 |
| C.金属晶体的熔、沸点均很高 | D.分子晶体中不一定含化学键 |
下列各组气体或溶液用括号内试剂加以鉴别,其中不合理的是
| A.二氧化碳、二氧化硫、一氧化碳(品红溶液) |
| B.氯化钠、硝酸银、碳酸钠(稀盐酸) |
| C.酒精、醋酸、醋酸钠(石蕊试液) |
| D.硫酸、硝酸钡、氯化钾(碳酸钠溶液) |
若1.8g某金属跟足量盐酸充分反应,放出2.24L(标准状况)氢气,则该金属是
| A.Mg | B.Al | C.Fe | D.Zn |