mA(g)+nB(g)  pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
| A.③④⑤⑥ | B.②③④⑥ | C.①③④⑤ | D.①③④⑥ |
仔细分析下列表格中每组醇与酸的关系,找出其关系的共同点,判断X的分子式为
| Ⅰ组[] |
Ⅱ组 |
Ⅲ组 |
Ⅳ组 |
||
| 醇 |
C2 H5 OH |
C4 H9 OH |
X |
CH3 CH(OH)— CH(OH)CH3 |
…… |
| 酸 |
HCOOH |
CH3 CH2 COOH |
H2 CO3 |
HOOC—COOH |
…… |
A.C3 H10 O B.C2 H6 O2C.C4 H10 O D.C3 H8 O2
燃烧等物质的量的某有机物和乙醇,①乙醇燃烧生成CO2的量是该有机物的2/3;②该有机物燃烧生成水的量是乙醇的2/3;③二者消耗相同状态下氧气的体积相同。通过分析判断该有机物是下列哪种( )
| A.C4 H9 OH | B.CH2 = CHCOOH |
| C.CH2=" CHCHO" | D.CH3 CH2 COOH |
甲苯在一定条件下与氢气完全加成生成甲基环己烷,该产物与氯气发生取代反应,生成的一氯代物有
| A.3种 | B.4种 | C.5种 | D.6种 |
历史上最早应用的还 原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是
原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是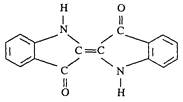
| A.靛蓝由碳、氢、氧、氮四种元素组成 |
| B.它的分子式是C16 H10 N2 O2 |
| C.该物质是高分子化合物 |
| D.它是不饱和的有机物 |
乙烯和1,3-丁二烯的混合气体1 L,催化剂存在下与足量氢气发生加成反应,消耗1.4 L氢气,则原混合气体中乙烯和1,3-丁二烯的体积比为
| A.3:2 | B.4:1 | C.3:1 | D.任意比 |